La rinitis aguda es un proceso inflamatorio que afecta a las vías respiratorias superiores y que se desarrolla en la mucosa nasal. En la actualidad, es una de las infecciones más frecuentes del cuerpo humano; los adultos padecen una media de entre 2 y 5 episodios al año, y, los niños, entre 8 y 12.
Los virus más frecuentemente relacionados con la rinitis aguda son los rinovirus, que causan prácticamente la mitad de los casos, seguidos por otros como los coronavirus, adenovirus, virus respiratorio sincitial (VRS), coxsackie, gripe y parainfluenza. Una vez que estos virus entran en contacto con la mucosa nasal, infectan las células epiteliales nasales, provocando daño de sus uniones intercelulares y alterando las membranas, lo que induce la muerte celular.
La clínica característica de la rinitis aguda vírica engloba una producción excesiva de moco con rinorrea, insuficiencia respiratoria nasal, estornudos, ojos llorosos y algún grado de prurito ocular y/o nasal. En el caso de los rinovirus, los síntomas suelen aparecer entre las 48 y 72 horas tras la inoculación, mientras que, en las infecciones causadas por otros virus, como el VRS, el cuadro clínico aparece a los 7 días tras el contagio. Aun así, el tiempo medio de resolución es de entre 4 y 10 días, sin existir diferencias entre los distintos virus.
Los síntomas nasales están desencadenados por el edema y la vasodilatación a nivel nasal. Tras la infección, la mucosa se hipertrofia, produciendo un exudado inflamatorio en forma de rinorrea hialina (transparente) o mucoide (verdosa-amarillenta). Tanto el edema como la vasodilatación, citados anteriormente, producen congestión nasal, que da lugar a una obstrucción mecánica al paso de aire. Por ello, los términos congestión nasal y obstrucción nasal se utilizan indistintamente en la mayoría de las ocasiones. Todos estos síntomas pueden llevar asociada una sintomatología sistémica caracterizada por fiebre, escalofríos o malestar general, que suele tener una duración media de 5 días. Por otra parte, la rinorrea hialina puede volverse mucopurulenta durante el desarrollo de la infección. Sin embargo, este hecho no se relaciona necesariamente con sobreinfección bacteriana, sino que se trata del progreso normal del proceso infeccioso.
En relación al tratamiento, aunque los estudios realizados han demostrado que la sintomatología se acorta cuando se lleva a cabo un tratamiento con antivirales, al ser la rinitis una infección con baja tasa de complicación y con una altísima incidencia, de forma sistemática únicamente se recomienda el tratamiento sintomático:
- Lavados nasales con soluciones salinas isotónicas o hipertónicas para disminuir la rinorrea.
- Incrementar la hidratación para compensar la respiración oral derivada de la insuficiencia respiratoria nasal.
- En caso de insuficiencia respiratoria nasal que ocasione sintomatología limitante para el paciente, pueden utilizarse vasoconstrictores nasales de forma tópica. Al existir el riesgo de efecto rebote, está recomendado que su utilización no exceda las 48-72 horas. Los vasoconstrictores nasales más eficaces y con mayor perfil de seguridad son los imidazoles, como oximetazolina y xilometazolina, aunque pueden utilizarse otros, como tramazolina o pseudoefedrina.
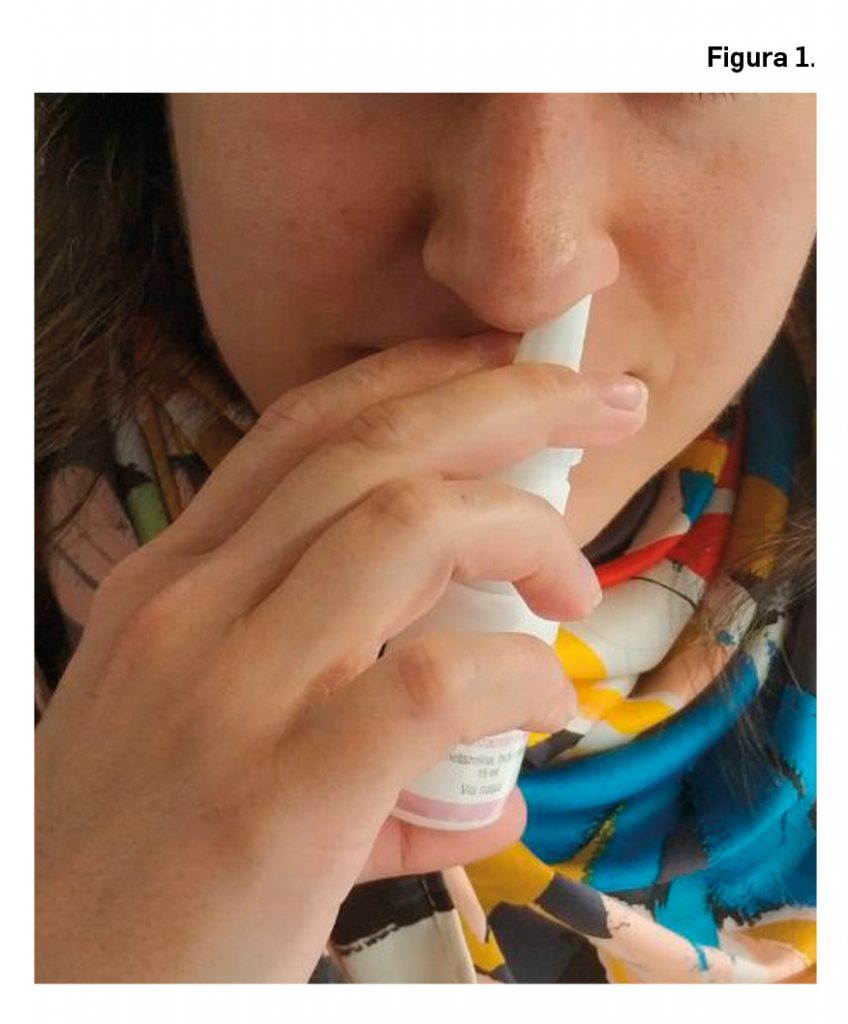
Algunos estudios insisten en la importancia de utilizar el vasoconstrictor nasal con el aplicador hacia arriba, puesto que al invertirlo puede aumentar de manera significativa la cantidad de fármaco dispensado en cada aplicación. Asimismo, se debe indicar a los pacientes que deben aplicarlo hacia la pared lateral nasal y no hacia el tabique nasal, pues de esta forma aumenta la eficacia del fármaco y disminuye la probabilidad de perforación del tabique. Una forma sencilla para no administrar el vasoconstrictor nasal directamente en el tabique nasal es aplicarlo con la mano contraria al orificio nasal, de esta forma siempre se aplicará en la pared lateral nasal (Figura 1).