La diabetes mellitus (DM) comprende un grupo de enfermedades metabólicas caracterizadas por hiperglucemia, y aparece como consecuencia de defectos en la secreción y/o acción de la insulina. La hiperglucemia crónica se asocia con lesiones a largo plazo en diversos órganos, particularmente ojos, riñón, nervios, vasos sanguíneos y corazón.
El síndrome metabólico (SM), por su parte, se caracteriza por la coincidencia en un sujeto de varios factores de riesgo cardiometabólico, fundamentalmente obesidad abdominal, hipertensión, dislipemia aterogénica e hiperglucemia.
Factores de riesgo
Los factores de riesgo para el desarrollo de DM o de SM son, en gran parte, comunes, y la resistencia a la insulina está en la base de su etiopatogenia. Destacan los siguientes:
- Etnia: la prevalencia es más alta en latinoamericanos, afroamericanos, americanos de origen asiático y oriundos de las islas del Pacífico.
- Edad: el envejecimiento parece estar íntimamente ligado a la aparición de DM.
- Sobrepeso/obesidad: el exceso de grasa corporal es el factor clave para el desarrollo de SM/DM.
- Sedentarismo: relacionado con lo anterior, una insuficiente actividad física contribuye a un balance calórico positivo y al acúmulo de grasa corporal.
- Hipertensión arterial y dislipemia: su papel se fundamenta en la existencia de resistencia a la insulina en una alta proporción de pacientes con estas patologías.
- Antecedentes familiares: se trata de contribuciones de múltiples genes, sobre los que actúan aspectos ambientales, que finalmente dan lugar a la aparición de SM/DM.
- Síndrome del ovario poliquístico y antecedentes de diabetes gestacional, macrosomía fetal o prediabetes.
Etiopatogenia
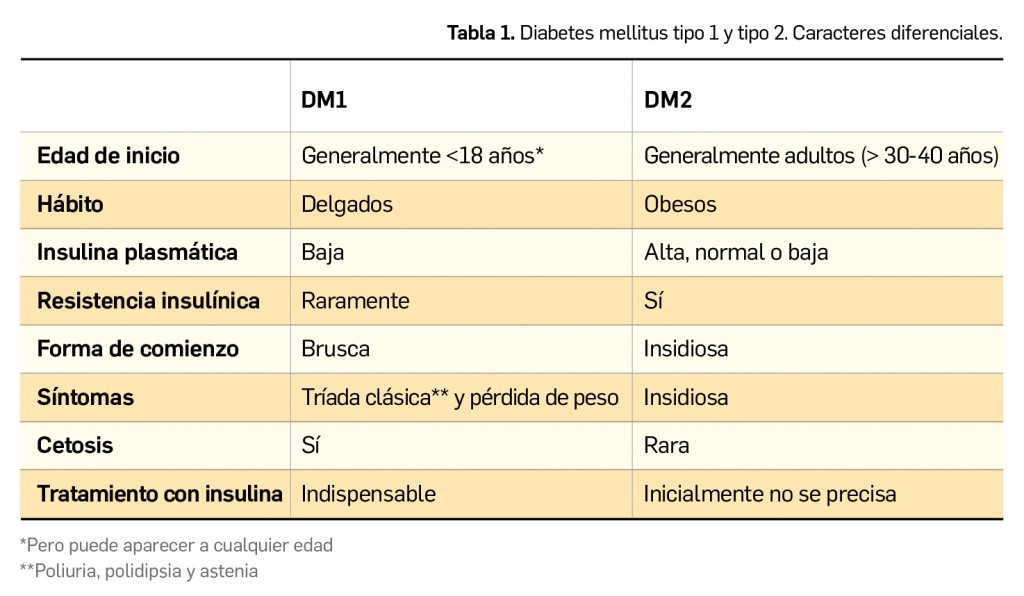
La DM1 es una enfermedad autoinmune que aparece tras la destrucción selectiva de las células β pancreáticas (productoras de insulina). En su etiología se entremezclan factores genéticos y ambientales (virus, dietéticos, toxinas, etc.). La autoinmunidad origina una producción de autoanticuerpos contra antígenos de las células β pancreáticas.
La DM2 está relacionada con la resistencia a la insuIina (RI), pero se requiere adicionalmente de un deterioro de la función de la célula β pancreática. Para compensar esa RI, la célula β pancreática produce más insulina, aunque con el tiempo no puede mantener esa capacidad y se produce hiperglucemia (Tabla 1).
Pronóstico
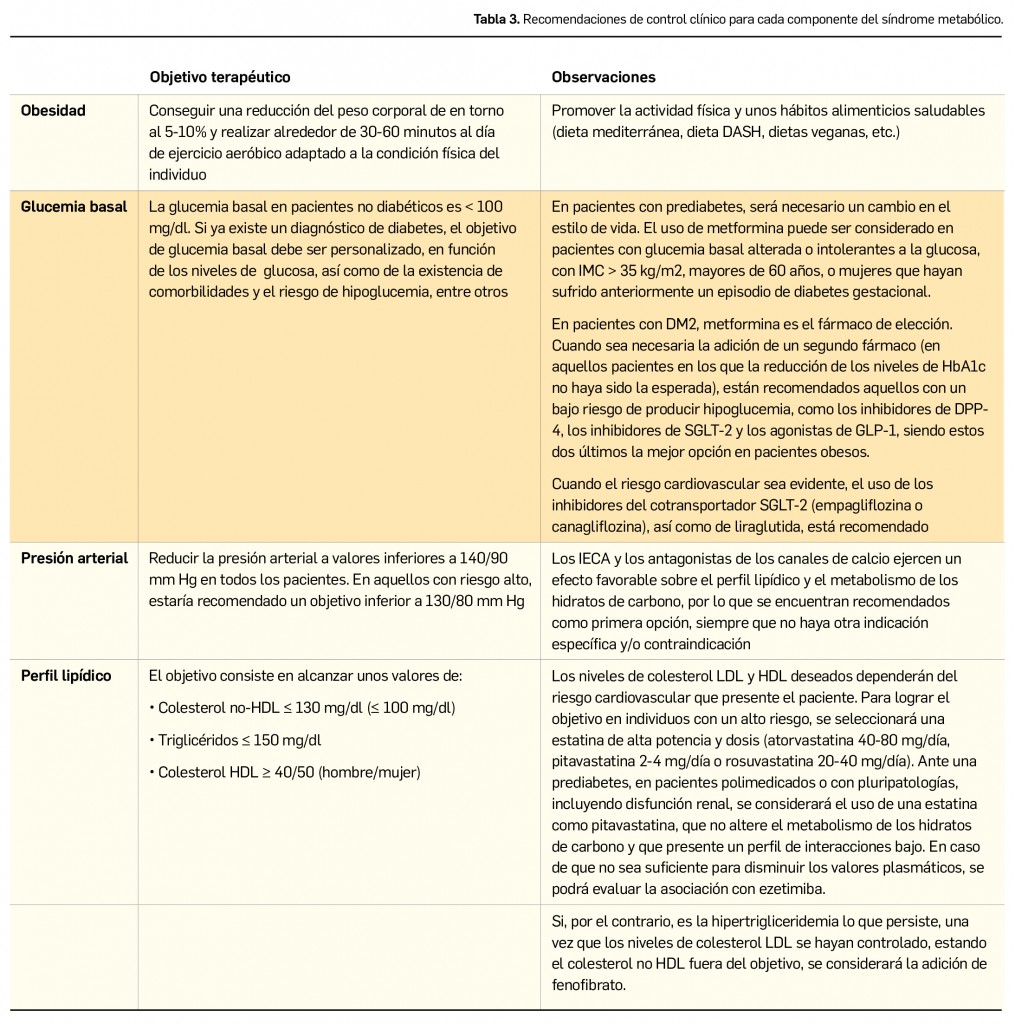
El pronóstico del paciente con DM depende fundamentalmente del grado de control de su enfermedad. Se recomienda mantener niveles de hemoglobina glucosilada (HbA1c) por debajo del 7% para evitar y/o retrasar la aparición de complicaciones microangiopáticas. En cuanto a estas complicaciones, además de al buen control glucémico, responden claramente al buen control del resto de factores de riesgo cardiovascular (control de la tensión arterial, de los lípidos, cese del tabaquismo, realización de ejercicio y alimentación equilibrada).
El pronóstico del SM depende del grado de control de los componentes que lo forman: un adecuado control de la tensión arterial, de los lípidos, de la glucosa y del peso.
Farmacoterapia de la DM1
El paciente con DM1 es insulinodeficiente y, en la actualidad, la insulina es su único tratamiento. Lo habitual es la administración de una o dos dosis de insulina lenta (para suministrar una cantidad de insulina basal) y la administración de tantas dosis de insulina rápida como ingestas haga el paciente, para controlar los niveles de glucemia postingesta (posprandial). Para el correcto ajuste de la dosis de insulina es necesario medir la glucemia (ayunas, antes de comer, de cenar y al acostarse).
Farmacoterapia de la DM2
Las intervenciones dirigidas a mejorar la actividad física del paciente y la alimentación son partes críticas en el tratamiento. Deben consumirse alimentos más saludables (más legumbres, verduras y vegetales, ricos en fibra, etc.) y realizar como mínimo 150 minutos por semana de actividad física moderada, que incluya actividad aeróbica, resistencia y entrenamiento de flexibilidad.
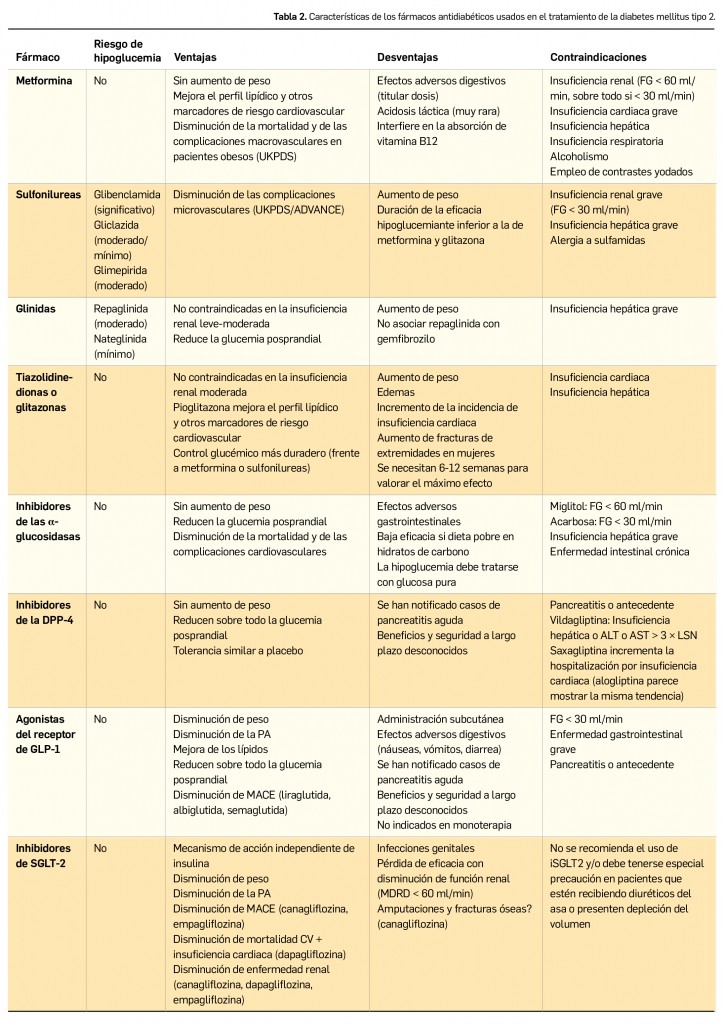
En pacientes motivados con una HbA1c alrededor del 7,5%, se puede dar una oportunidad a la modificación del estilo de vida durante un periodo de 3-6 meses antes de iniciar el tratamiento farmacológico. Si la hiperglucemia es moderada, o si se prevé que la modificación del estilo de vida no dará resultado, se iniciará tratamiento farmacológico (Tabla 2) desde el diagnóstico (generalmente metformina), que podrá ser modificado o suspendido posteriormente. En el caso de que no se pueda utilizar metformina, podrá elegirse otro fármaco oral (sulfonilurea/glinida, pioglitazona, iDPP-4, arGLP-1 o iSGLT-2).
En pacientes con hemoglobina glucosilada elevada de inicio, suele ser necesario iniciar el tratamiento con insulina, sola o asociada con metformina. Algunas guías de práctica clínica recomiendan empezar con doble terapia de inicio, cuando la HbA1c es mayor del 7,5%, y la doble o triple terapia o insulina (paciente sintomático), cuando dicho valor es mayor del 9%.
Si con metformina en monoterapia no se controla la glucemia, se debería añadir un segundo fármaco oral, un agonista del receptor de GLP-1 (arGLP-1) o insulina basal. A mayor HbA1c, más probable será la necesidad de iniciar tratamiento con insulina. Se recomienda que los fármacos asociados tengan un mecanismo de acción diferente y complementario.
La asociación de metformina con sulfonilureas es la combinación más estudiada y ha demostrado su eficacia y seguridad, aunque su uso está asociado a una mayor tasa de hipoglucemias y de aumento de peso. Las glinidas constituyen una buena alternativa a las sulfonilureas en pacientes con ingestas más irregulares por su corto periodo de acción.
Los inhibidores de la dipeptidilpeptidasa-4 (iDPP-4) presentan ventajas evidentes frente a las sulfonilureas y las glinidas en relación al bajo riesgo de hipoglucemias y su neutralidad en el peso. En los últimos años se han posicionado como la principal alternativa tras el fracaso de metformina en monoterapia, desplazando a las sulfonilureas del segundo escalón terapéutico, especialmente en pacientes con alto riesgo de hipoglucemia, y son la recomendación preferente en el paciente anciano.
Los arGLP-1 son preparados de administración subcutánea que consiguen un efecto sobre los receptores de arGLP-1 más intenso y prolongado que el logrado por los iDPP-4. Ayudan a mejorar el control glucémico, inducen pérdida de peso y reducciones de la presión arterial.
Las tiazolidinedionas o glitazonas mejoran la sensibilidad a la insulina en el tejido muscular esquelético y reducen la producción hepática de glucosa. Su indicación se centra en pacientes con un buen control posprandial de la glucemia y con elevación de la glucemia basal que no se corrige totalmente con metformina.
Los inhibidores de las α-glucosidasas retrasan la digestión de los hidratos de carbono con reducción de los picos glucémicos posprandiales. Su asociación con metformina es segura, ya que no se van a producir hipoglucemias, pero su eficacia es muy limitada.
Los iSGLT-2, además de ayudar a mejorar el control glucémico, también inducen pérdida de peso (en menor cuantía que los arGLP-1) y reducción de la presión arterial.
En la triple terapia, la recomendación más importante es utilizar fármacos con mecanismos de acción complementarios. La asociación de metformina, sulfonilurea y pioglitazona es la más estudiada y utilizada en la práctica asistencial. Otras opciones son la asociación de metformina, repaglinida y glitazona, así como la de metformina, glitazona y un iDPP-4. En aquellos pacientes con limitaciones para el uso de las tiazolidinedionas, las alternativas más razonables serían metformina más sulfonilureas más un iDPP-4, o metformina más repaglinida más un iDPP-4.
Diabetes gestacional
El tratamiento se basa en el seguimiento de un adecuado plan de alimentación. Si no se cumplen los objetivos glucémicos, hay que recurrir al tratamiento con insulina.
Terapias extrafarmacológicas
En el caso de la DM1 pueden plantearse como opciones extrafarmacológicas el trasplante pancreático (TP), el trasplante de islotes (TI) o la terapia celular.
En la DM2 son fundamentales la dieta y el ejercicio. La cirugía bariátrica ha supuesto también una importante alternativa de tratamiento para los pacientes con obesidad mórbida y DM2.
Conceptos clave
– La consecución de un buen control metabólico puede evitar o retrasar la aparición de las complicaciones micro- y macroangiopáticas. Conseguir un valor de HbA1c inferior al 7% ha demostrado reducir las complicaciones microangiopáticas de la diabetes.
– La DM1 se caracteriza por debutar con una serie de síntomas cardinales: polidipsia, poliuria, polifagia, pérdida de peso y astenia, que ocurren como consecuencia de la diuresis osmótica, hipertonicidad del medio interno e imposibilidad para traslocar los transportadores GLUT para importar los glúcidos ingeridos.
– El tratamiento en pacientes con DM1 suele ser de múltiples dosis diarias de insulina, consistente generalmente en 4 dosis de insulina (1 de lenta y 3 de rápida).
– En los pacientes con DM2, son fundamentales las intervenciones dirigidas a mejorar la actividad física del paciente y la alimentación.
– Metformina es el fármaco de elección para el inicio del tratamiento farmacológico. Si no se puede utilizar metformina, debe elegirse otro fármaco oral, como una sulfonilurea/glinida, pioglitazona, un inhibidor de la enzima dipeptidil peptidasa 4 (iDPP-4), un agonista del receptor del péptido 1 similar al glucagón (arGLP-1) o un inhibidor del cotransportador sodio-glucosa tipo 2 (iSGLT-2).
– Si el tratamiento con metformina en monoterapia no consigue alcanzar o mantener el objetivo de HbA1c en 3 meses, se debería añadir un segundo fármaco oral, un arGLP-1 o insulina basal.