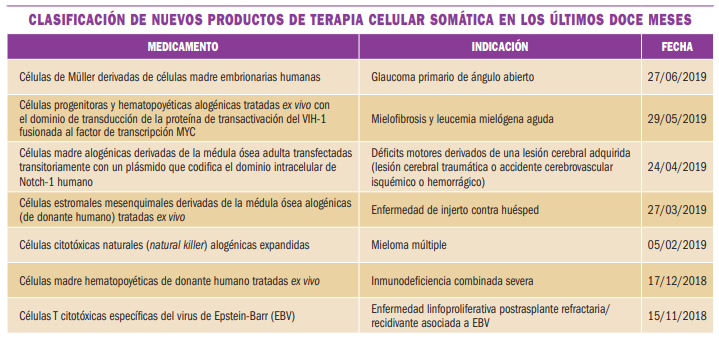
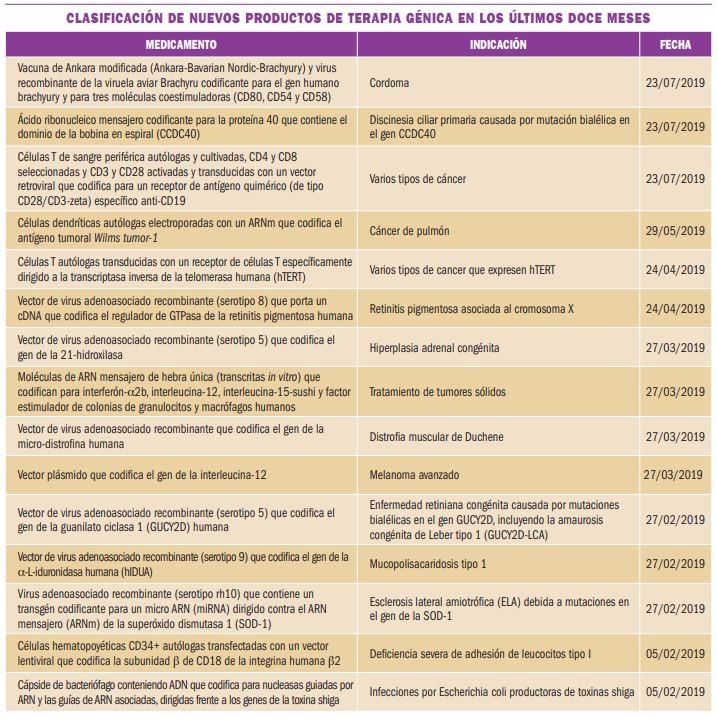
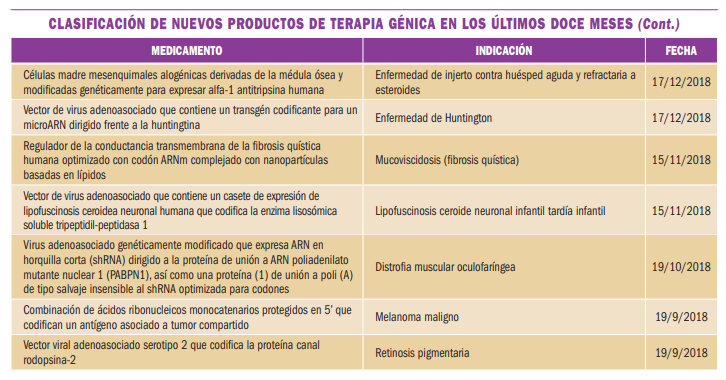
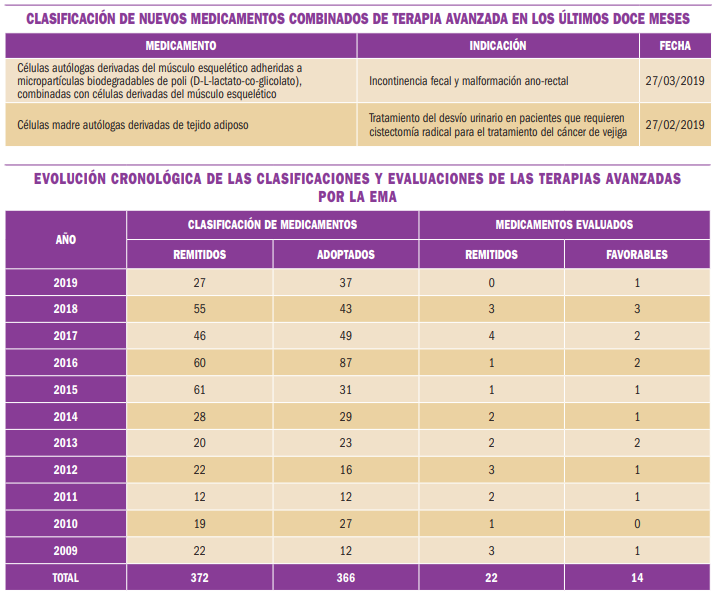
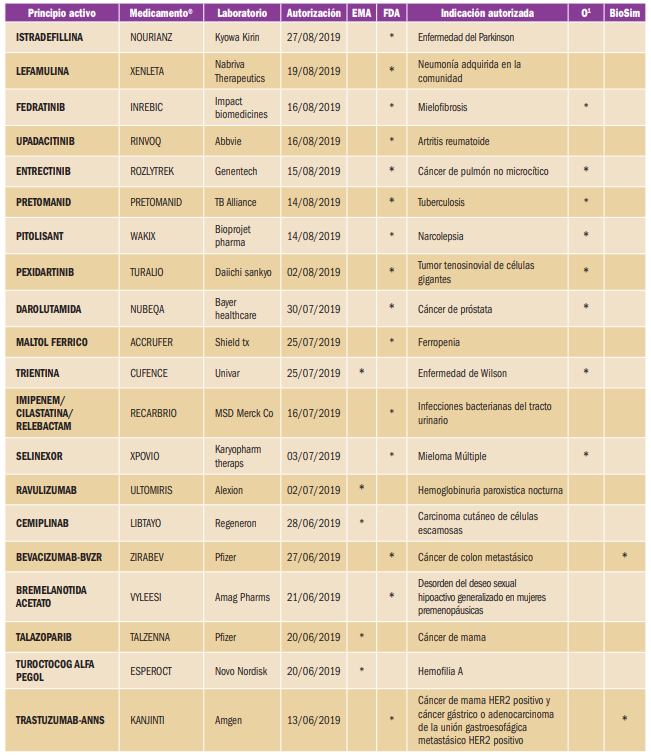
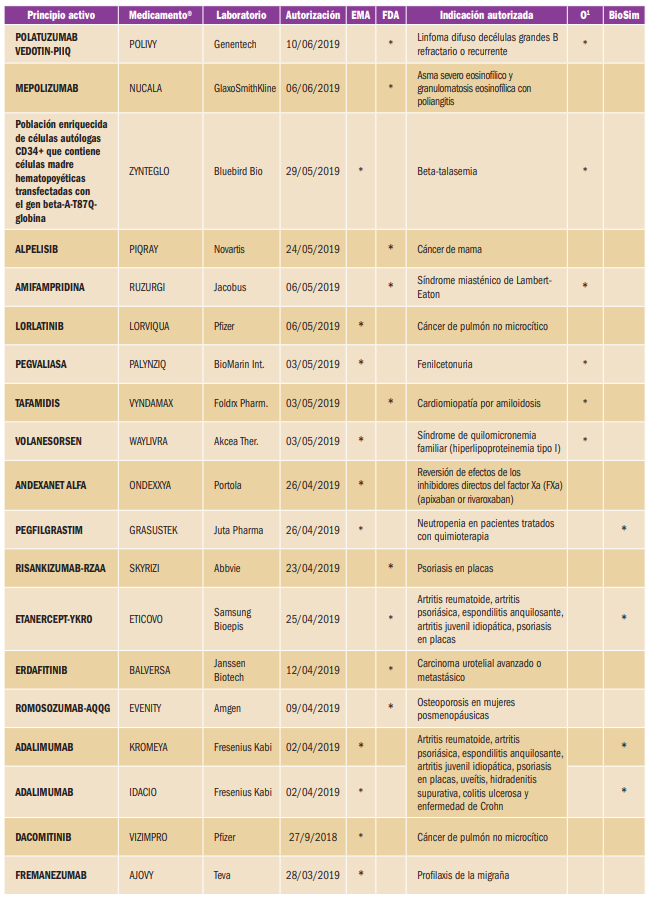
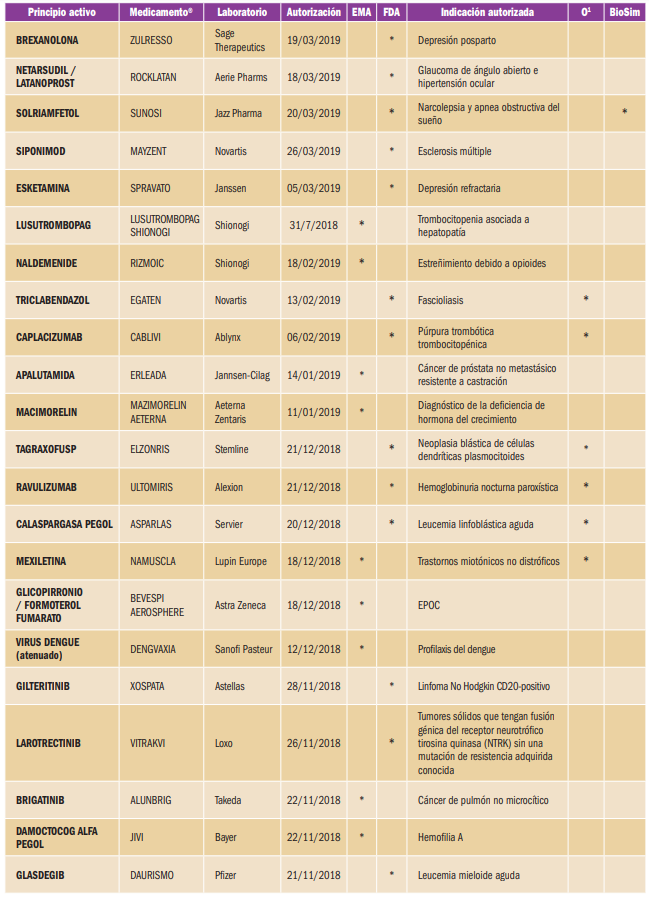
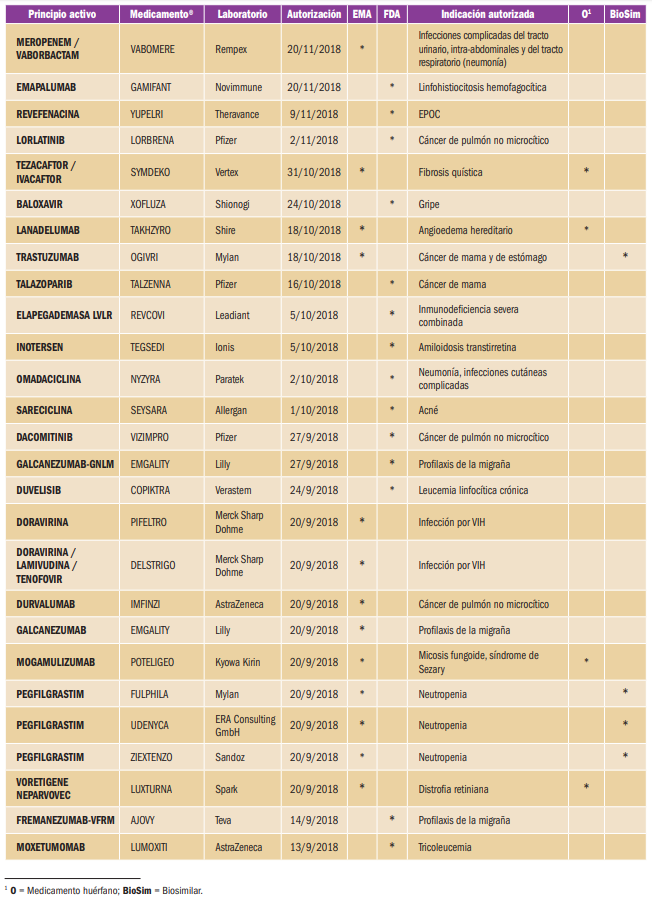
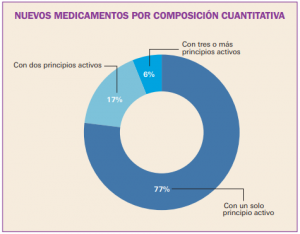
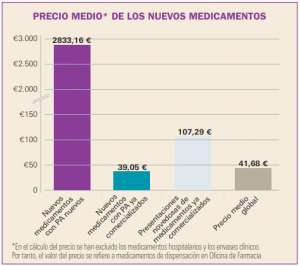
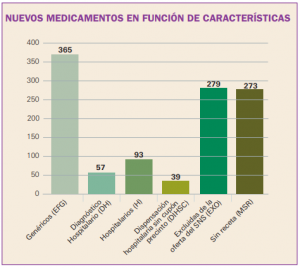
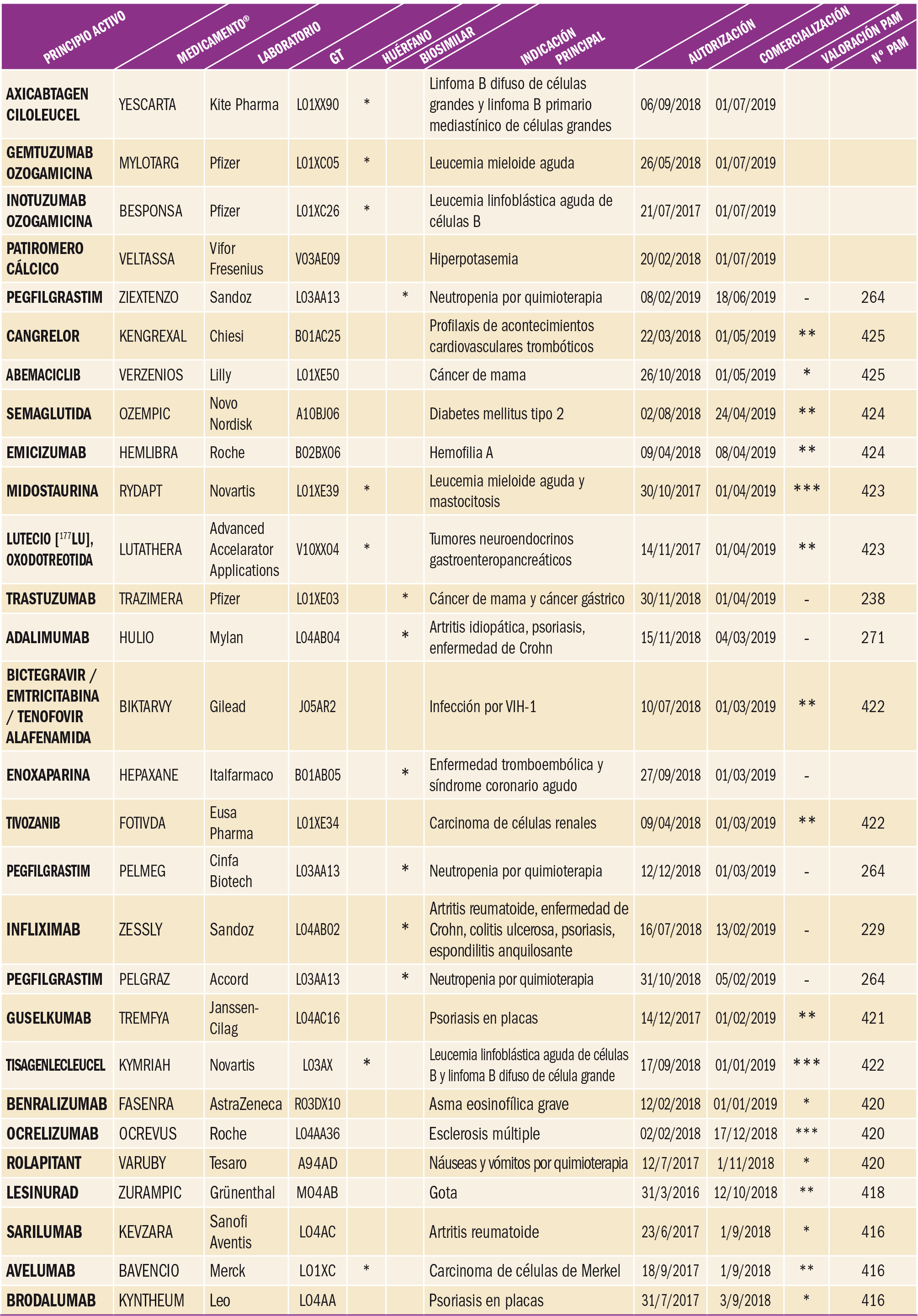
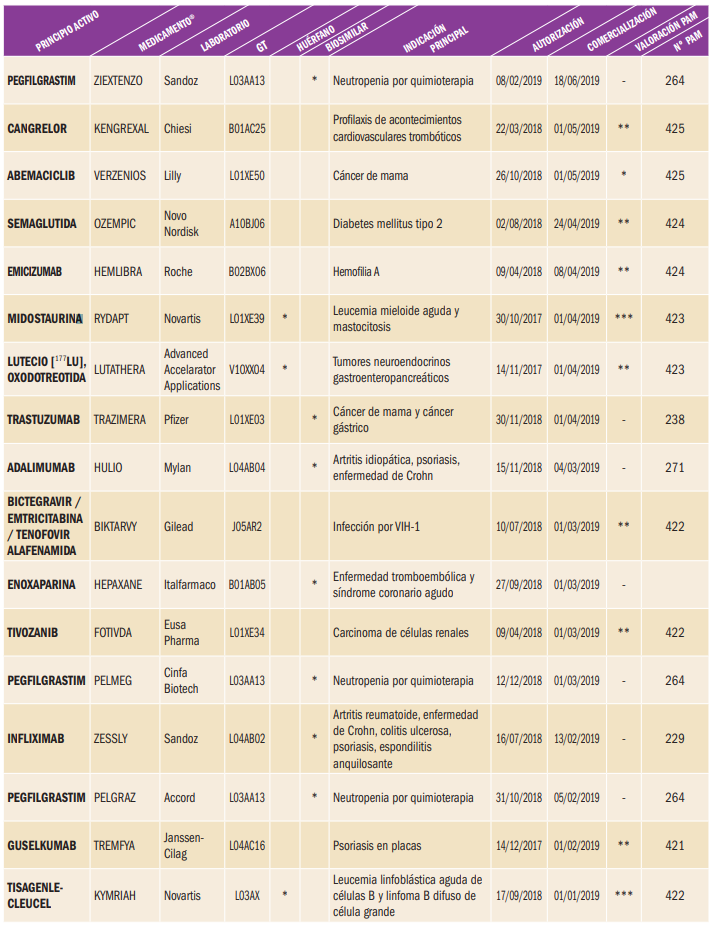
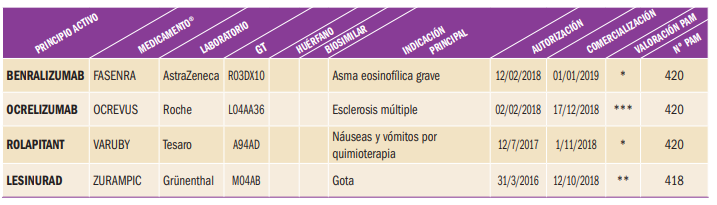
NUEVOS MEDICAMENTOS HUÉRFANOS
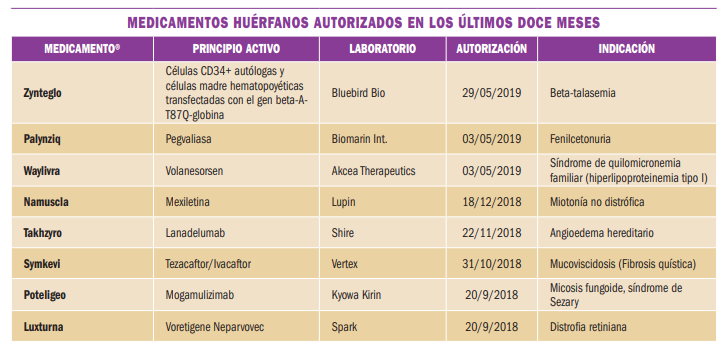
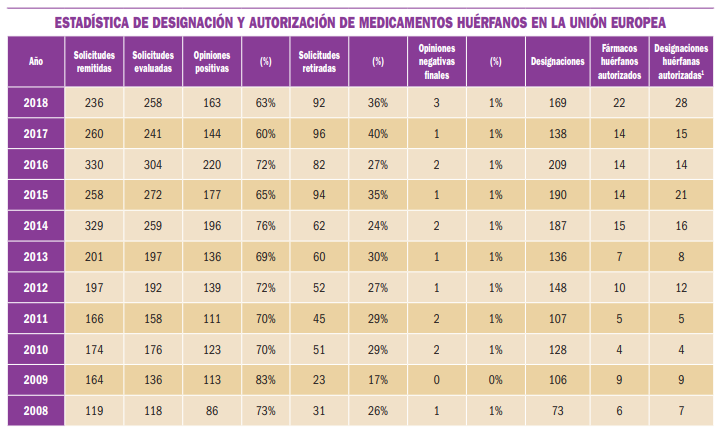
Los medicamentos huérfanos son aquellos que sirven para diagnosticar, prevenir o tratar enfermedades raras de carácter muy grave o con riesgo para la vida. En la Unión Europea, la calificación de enfermedad rara se aplica a todas aquellas que no afectan a más de 5 de cada 10.000 personas. La designación de un medicamento como huérfano no garantiza su uso en la condición designada y no implica necesariamente que el producto satisfaga los criterios de eficacia, seguridad y calidad necesarios para la concesión de la autorización de comercialización. Como para cualquier medicamento, estos criterios sólo pueden ser evaluados una vez que la solicitud de autorización de comercialización haya sido presentada.
PUBLICACIONES Y PÁGINAS WEB DE INTERÉS
A) Instituciones y redes españolas
instituto de salud carlos iii (Ministerio de Ciencia e Innovación):
– Instituto de Enfermedades Raras:
– CIBERER (Centro de Investigación Biomédica en Red de Enfermedades Raras):
http://www.isciii.es/htdocs/centros/enfermedadesraras/enfermedadesraras_presentacion.jsp
Instituto de Mayores y Servicios Sociales (IMSERSO, Ministerio de Sanidad, Política Social e Igualdad):
http://www.imserso.es/imserso_01/index.htm
Federación Española de Enfermedades Raras (FEDER)
www.enfermedades-raras.org
– Asociaciones de pacientes en España:
http://www.feder.org.es/asociaciones_listado.php
B) Instituciones y redes europeas
Agencia Europea de Medicamentos (EMA; Europea Medicines Agency). Apartado de Medicamentos
Huérfanos (Inglés):
Comisión Europea: web oficial de la Comisión Europea sobre enfermedades raras y medicamentos
huérfanos (español).
http://ec.europa.eu/health/rare_diseases/policy/index_es.htm
Orphanet: Portal de información oficial de la Unión Europea sobre enfermedades raras y medicamentos huérfanos (español).
http://www.orpha.net/consor/cgi-bin/index.php?lng=ES
Eurordis: Federación Europea de Asociaciones de Pacientes con Enfermedades Raras (español).
http://www.eurordis.org/es
C) Otras instituciones y redes internacionales
Food & Drug Administration (FDA, Estados Unidos). Apartado de Medicamentos Huérfanos (inglés):
http://www.fda.gov/ForIndustry/DevelopingProductsforRareDiseasesConditions/default.htm
Pharmaceuticals & Medical Devices Agency. Agencia de Medicamentos y Dispositivos Médicos, de Japón (inglés):
http://www.pmda.go.jp/english/index.html