|
EVENTO |
FECHA |
INFORMACIÓN |
LOCALIDAD |
DIRECCIÓN POSTAL |
DIRECCIÓN TELEMÁTICA |
|---|---|---|---|---|---|
|
XIX CONGRESO NACIONAL FARMACÉUTICO
|
22-24 de octubre de 2014 |
CONGRAL |
Córdoba |
|
Tel: 91 431 25 60 |
|
21-23 de noviembre de 2014 |
|
Suzhou China |
|
|
|
|
2-3 de diciembre de 2014 |
|
Berlin Alemania |
|
Tel:: +41 61 225 51 51 Fax: +41 61 225 51 52 |
|
|
XII CONGRESO DE LA SOCIEDAD DE FARMACIA INDUSTRIAL Y GALENICA
|
26-28 de enero de 2015 |
SEFIG Facultad de Farmacia de Barcelona |
Barcelona |
|
|
|
PHARMACOVIGILANCE AND RISK MANAGEMENT STRATEGIES 2015 |
26-28 de enero de 2015 |
|
Washington, DC Estados Unidos |
|
Tel: +1.215.442.6100 |
|
10 de marzo de 2015 |
|
Bruselas Bélgica |
|
Tel:+32 2 709 01 42 |
|
|
INFARMA 2015: CONGRESO EUROPEO DE FARMACIA, MEDICAMENTOS Y PARAFARMACIA |
24-26 de marzo de 2015 |
|
Barcelona |
|
|
|
THE EUROPEAN ASSOCIATION OF HOSPITAL PHARMACISTS (EAHP)
|
25-27 de marzo de 2015 |
EAHP |
Bruselas Bélgica |
|
Tel:+32 (0) 2/741.68.29 Fax:+32 (0) 2/734.79.20 |
|
13-14 de abril de 2015 |
|
Reims Francia |
|
Tel: 49/6131/9767-0 Fax: 49/6131/9767-69 |
|
|
20-22 de abril de 2015 |
DIA |
North Bethesda Estados Unidos |
|
Tel: +1.215.442.6100 Fax +1.215.442.6199 ETCustomerService@diahome.org |
|
|
28 de septiembre -3 de octubre de 2015 |
FIP |
Dusseldorf Alemania |
|
|
Archive
Revista PAM: 377
Número 377, Octubre 2014
Plan Nacional de Formación Continuada
La psoriasis es una enfermedad crónica de la piel de carácter inflamatorio, una de sus principales manifestaciones es la hiperqueratosis paraqueratósica de la epidermis. Puede afectar a la piel, uñas, articulaciones y, menos frecuentemente, a las mucosas.
La lesión característica es una placa de color rojo oscuro, con escamas no adherentes de un peculiar tono blanco-nacaradas y con borde bien delimitado. Se manifiesta habitualmente de forma bilateral, siendo las localizaciones más frecuentes las superficies de extensión articular (codos y rodillas), la zona sacra y el cuero cabelludo. La afectación de las mucosas es muy rara, aunque se han citado casos localizados en los labios y en el pene.
La psoriasis es la más común de las enfermedades cutáneas crónicas humanas, con una incidencia del 2% en la población mundial. Puede comenzar a cualquier edad, pero es rara en menores de 5 años. Presenta dos picos de máxima incidencia: la segunda década (de origen generalmente familiar) y los 55-60 años. Evoluciona con remisiones y recaídas espontáneas. Puede persistir toda la vida o durar solo unos meses. Aunque muy raramente llega a poner en peligro la vida del paciente, puede ser muy discapacitante, limitando considerablemente la calidad de vida.
Entre las principales características histológicas de la psoriasis pueden citarse la hiperplasia epidérmica, definida como una diferenciación anormal y la maduración incompleta de los queratinocitos; un engrosamiento de la epidermis y una capa granular reducida o ausente. Todo ello es debido a la hiperproliferación y diferenciación de queratinocitos epidérmicos de evolución acelerada, cuyo ciclo vital es mucho más rápido de lo normal: tardan 7-10 días en lugar de 50-75 días. También se puede apreciar una infiltración epidérmica de células del sistema inmune (linfocitos T) y de células dendríticas CD11c+ en la dermis; por otro lado, se encuentran células CD8+ y neutrófilos en la epidermis. Hoy se considera que la psoriasis es una enfermedad inflamatoria crónica de origen autoinmune en la cual células dendríticas, linfocitos T, macrófagos y neutrófilos inducen hiperproliferaciones locales de queratinocitos que, en última instancia, son las responsables de las lesiones de la piel.
La forma clínica más frecuente (hasta el 80% de los casos) es la psoriasis vulgar o en placas. Este último término hace referencia a las formaciones escamosas y de color rojizo presentes en las zonas de extensión (codos y rodillas, principalmente), así como en el cuero cabelludo.
La psoriasis se asocia con un aumento del riesgo de la aterosclerosis y del riesgo de enfermedad cardiovascular, que se asocia con mayores tasas de morbilidad y mortalidad, especialmente en los pacientes de psoriasis más jóvenes y con formas más graves de la enfermedad, reduciendo su esperanza de vida.
El tratamiento de la psoriasis es complejo, ya que no solo se lucha contra una enfermedad de etiología desconocida y con formas clínicas muy diversas, sino que está condicionada por diversos factores sociales. Deben evitarse los factores desencadenantes y favorecedores conocidos: infecciones, golpes, tabaquismo y estrés. El sol es beneficioso, siendo capaz de producir una mejoría significativa de las lesiones; sin embargo, no existen evidencias sobre la posible eficacia de otros tratamientos no farmacológicos.
No existe un tratamiento curativo para la psoriasis, pero en la mayoría de los casos puede controlarse satisfactoriamente, aplicando diferentes tratamientos en función de la gravedad del caso.
Los tratamientos tópicos son empleados en los casos más leves (afectación menor del 25% de la superficie corporal) y constituyen la forma más común de tratamiento de la psoriasis en placas, pero también es la menos eficaz en los casos graves. Carecen de utilidad en la artritis psoriásica o en la forma pustulosa y en la eritrodérmica.
Los agentes emolientes y queratolíticos (ácido salicílico, brea de hulla, ditranol) son utilizados habitualmente como adyuvantes a otros tratamientos para hidratar, evitar la aparición de fisuras y eliminar las escamas. Por su parte, los corticosteroides tópicos producen efectos rápidos y potentes, pero la duración de las remisiones es más bien corta. Se pueden considerar de primera elección en la psoriasis leve que no responde a otros tratamientos tópicos y en determinadas localizaciones como la cara, el cuero cabelludo, los pliegues, los genitales (localizaciones que no toleran otros tratamientos tópicos).
El calcipotriol y el tacalcitol son análogos hormonales de la vitamina D de aplicación tópica, similares al calcitriol. Su empleo en la psoriasis en placas se debe a la observación de que los análogos hormonales de la vitamina D son capaces de inhibir la proliferación y la diferenciación de los queratinocitos. Su eficacia es similar a la de los corticosteroides e incluso inducen periodos de remisión algo más largos que aquellos.
El empleo de lámparas de radiación ultravioleta (UV) constituye uno de los puntales en el tratamiento de la psoriasis. Sin embargo, la aplicación de radiación UV solo resulta útil en los casos de psoriasis en placas, resultando ineficaz en el resto de formas de psoriasis (artritis, etc.). El método PUVA o fotoquimioterapia es el tratamiento más eficaz disponible para la psoriasis en placas. Su acción es lenta, pero produce periodos prolongados de remisión. Debido al riesgo de efectos adversos cutáneos se está empleando de forma mucho más restringida, para casos graves refractarios en pacientes de edad media (no en niños ni en jóvenes). Algo menos eficaz es la fototerapia. Se suele emplear brea de hulla previamente a la radiación UVB.
El tazaroteno es un retinoide que se utiliza por vía tópica. En los pacientes con psoriasis en placas presenta un eficacia similar a la de los corticosteroides tópicos en lo que se refiere a la elevación de las placas psoriásicas, pero su efecto es algo menor en cuanto a la reducción del eritema. La combinación de tazaroteno y corticosteroides produce mejores resultados que el tazaroteno solo.
En el tratamiento sistémico se emplean agentes con efectos antiproliferativos sobre la epidermis. Se trata de fármacos inmunosupresores y derivados retinoides aromáticos. Son considerados como el segundo nivel de tratamiento, estando indicados en psoriasis extensas que no responden a otros tratamientos, formas eritrodérmicas y pustulosas y formas incapacitantes.
Los denominados fármacos antirreumáticos modificadores de la enfermedad (FAME o DMARD, disease-modifiying antirheumatic drugs) son ampliamente utilizados como primera opción en el tratamiento de las formas activas moderadas o graves de la psoriasis, en particular en los pacientes con artritis psoriásica. Se trata de potentes inmunosupresores, entre los cuales el más utilizado es, sin duda, el metotrexato, considerado como el tratamiento de elección en las formas graves de psoriasis en placas, así como en la artritis psoriásica, la psoriasis pustulosa y la psoriasis eritrodérmica. La hidroxiurea también se utiliza en esta indicación, pero es menos eficaz y su acción es más lenta que la del metotrexato; además, esta indicación no está oficialmente autorizada. Por su parte, la ciclosporina tiene una eficacia clínica similar a la del metotrexato en la psoriasis en placas y en la psoriasis pustulosa, pero algo menor en la psoriasis eritrodérmica y en la artritis psoriásica. Se utiliza en dosis muy inferiores a las empleadas en la prevención del rechazo en trasplante de órganos.
Los retinoides son análogos estructurales de la vitamina A (ácido retinoico), pero de carácter aromático. Actúan sobre receptores específicos, reduciendo la producción de estímulos inflamatorios y la diferenciación y proliferación de los queratinocitos. Revierten los cambios típicos hiperqueratósicos de la psoriasis en placas. Se utilizan actualmente el etretinato y la acitretina.
Los fármacos biológicos tienen como objetivo bloquear a determinadas citocinas implicadas en la génesis y/o progresión de la psoriasis. Han superado notablemente la eficacia y, especialmente, la seguridad de los tratamientos sistémicos previos. Sin embargo, sus efectos a largo plazo, tanto en relación con su eficacia como –especialmente– su seguridad, tienen que ser investigados más a fondo. El factor de necrosis tumoral alfa (TNF∝) es una citocina extremadamente proinflamatoria y muy relevante en el desarrollo de la inflamación en la psoriasis. De hecho, estimula la producción de citocinas y la adhesión de moléculas por los queratinocitos y, por lo tanto, aumenta el reclutamiento de células inmunes.
Los fármacos anti-TNF actualmente comercializados en España que están indicados expresamente en la psoriasis son infliximab, etanercept y adalimumab. Otros agentes anti-TNF disponibles en nuestro país son el golimumab, que está indicado en la artritis psoriásica, la artritis reumatoide, la colitis ulcerosa y la espondilitis anquilosante, y el certolizumab pegol, que está indicado para la artritis psoriásica, la artritis reumatoide, la espondilitis anquilosante y la espondiloartritis.
Por otro lado, el ustekinumab es un anticuerpo monoclonal humanizado frente a las interleucinas IL-12 y IL-23, autorizado para el tratamiento de la psoriasis en placas moderada o grave en adultos que no responden, tienen contraindicada o no toleran otras terapias sistémicas, incluyendo metotrexato, ciclosporina y PUVA. La IL-12 y la IL-23 contribuyen a la activación de los linfocitos natural killers (NK) y a la activación y diferenciación de los linfocitos CD4+, y su regulación parece estar alterada en pacientes con psoriasis y otras patologías de etiología autoinmune.
|
INFORMACIÓN DE INTERÉS |
||
|---|---|---|
|
Información e inscripciones (Centro de atención telefónica) |
||
|
902 460 902 / 91 431 26 89 |
9:00-19:00 h., de lunes a viernes |
|
|
Línea Directa del PNFC(1): |
||
|
91 432 81 02 |
9:00 a 14:00 h., de lunes a viernes |
|
|
Secretaría Técnica Administrativa(2): |
||
|
91 432 41 00 / Fax 91 432 81 00 |
L-J: 9:00-14:00 / 16:30-18:00 h / V: 9:00-14:00 |
|
(1) Consultas sobre contenidos técnico-científicos.
(2) Consultas sobre corrección de exámenes y certificados.
|
Direcciones DE INTERÉS |
|
|---|---|
|
Cuestionarios / Sugerencias |
CGCOF / PNFC: C/ Villanueva, 11, 7.º – 28001 Madrid |
|
Sección de Formación en Portalfarma |
|
|
Plataforma de formación on line |
|
|
CURSOS |
|||
|---|---|---|---|
|
CALENDARIO PREVISTO DEL PLAN NACIONAL DE FORMACIÓN CONTINUADA CONSEJO GENERAL DE COLEGIOS OFICIALES DE FARMACÉUTICOS |
|||
|
Curso |
Plazos de |
|
|
|
Terapéutica farmacológica de los trastornos de los aparatos respiratorio, osteomuscular y genitourinario (2ª edición) |
Cerrada |
16/7/14 |
16/1/15 |
|
Terapéutica farmacológica de los trastornos dermatológicos, oftalmológicos y otológicos. Agentes farmacológicos de diagnóstico |
Hasta 30/9/14 |
27/10/14 |
27/4/15 |
|
Búsqueda y manejo de información en Bot PLUS 2.0 (2ª Ed) |
Hasta 14/10/14 |
20/10/14 |
20/1/15 |
|
Sistemas personalizados de dosificación (3ª Ed) |
Cerrada |
1/10/14 |
2/12/14 |
|
Búsqueda y manejo de información en Bot PLUS 2.0 (3ª Ed) |
Hasta 20/1/15 |
26/1/15 |
27/4/15 |
|
Investigación en farmacia asistencial |
Cerrada |
26/5/14 |
27/2/15 |
|
CURSOS Y ACREDITACIÓN DEL PLAN NACIONAL DE FORMACIÓN CONTINUADA |
|
|---|---|
|
Terapéutica farmacológica de los trastornos dermatológicos, oftalmológicos y otológicos. |
Pendiente |
|
Terapéutica farmacológica de los trastornos del aparato digestivo, metabolismo y sistema endocrino |
13,8 |
|
Terapéutica farmacológica de los trastornos de los aparatos respiratorio, osteomuscular y genitourinario |
13,7 |
|
Sistemas personalizados de dosificación |
3,9 |
|
Farmacovigilancia |
13,8 |
|
Búsqueda y manejo de información en Bot PLUS 2.0 |
4 |
|
Buenas prácticas de distribución farmacéutica |
6 |
|
Investigación en farmacia asistencial |
Pendiente |
(*) Acreditados por la Comisión de Formación Continuada del Sistema Nacional de Salud.
Revisiones de artroplastia de cadera: motivos y componentes protésicos implicados
Resumen
La fractura de cadera es una de las causas más frecuentes de ingreso hospitalario, resultando la prótesis total de cadera uno de los mayores adelantos en cirugía ortopédica del siglo pasado, ofreciendo una mejora notable en la capacidad funcional de los pacientes con artropatías.
Los objetivos principales son, evaluar los principales motivos de revisión de artroplastia de cadera, identificar componentes implicados en las revisiones y estudiar la duración de los diversos componentes protésicos implantados. Para obtener esta información, se consultaron las historias clínicas de todos los pacientes sometidos a revisión de artroplastia de cadera desde enero de 2009 hasta agosto de 2013.
Los motivos desencadenantes de una revisión protésica fueron, de mayor a menor: AA, AS, LUX y FP. Los componentes no cementados fueron los más frecuentemente implicados en AA., concretamente los cotilos no cementados. En todos los casos de AS., estuvieron implicados componentes protésicos no cementados. El componente que con más frecuencia se luxó fue la cabeza femoral no cementada. La prótesis que con más frecuencia se implantó en la primera intervención fue el modelo Zweymuller y en las sucesivas revisiones, la prótesis total modelo Solution y los injertos de hueso. En la mayoría de los casos, entre la implantación de la prótesis original y la primera revisión transcurrieron entre 6 y 10 años. Los grupos de población mayoritariamente sometidos a revisión fueron: pacientes con sobrepeso, las mujeres y los pacientes entre 61 y 70 años. El tiempo medio de ingreso hospitalario fue de 14,5 días.
Introducción
La sustitución de la articulación de la cadera o artroplastia, es un procedimiento quirúrgico mediante el cual se sustituye total o parcialmente la articulación afectada, por una artificial, llamada prótesis. Cuando lo que se sustituye es una prótesis de cadera colocada previamente, se habla de revisión.
La prótesis total de cadera ha sido descrita como uno mayores adelantos de la cirugía ortopédica del siglo pasado1. En las últimas décadas, los reemplazamientos quirúrgicos articulares han supuesto una importante mejora en la capacidad funcional de los pacientes con artropatías. En nuestro país, se colocan anualmente alrededor de 30.000 prótesis articulares, la mayoría de rodilla y cadera, y en todo el mundo más de 1 millón2, sin embargo, el aumento progresivo de la esperanza de vida en la población occidental propicia el incremento cada vez mayor de estas cifras.
La incidencia de fracturas femorales proximales en mujeres es de 2 a 3 veces superior que en hombres3,4. La media de edad de los pacientes con fractura de cadera se ha incrementado en las 2 últimas décadas, situándose entre 82 a 87,5 años5.La duración estimada de una prótesis de cadera se sitúa en torno a 10-15 años6, aunque algunas sobrepasan este tiempo o en otras, su duración es mucho menor.
Existen diversos estudios que establecen cuáles son las causas fundamentales de reemplazamiento protésico7,8,9. Según una revisión publicada en Internacional Orthopaedics, el principal motivo de recambio de artroplastia de cadera, correspondió a aflojamiento aséptico, seguido de infección, inestabilidad, fallo de componente, fractura periprotésica y dolor.7
Sin embargo, resulta complicado encontrar una estadística que refleje por qué los pacientes son intervenidos de revisiones de artroplastia de cadera en los diversos centros hospitalarios nacionales, así como los materiales reemplazados y los de nuevo implante, con datos referentes a su duración y a las características de los pacientes portadores.
- Objetivos principales del estudio: Evaluar los principales motivos de revisión de artroplastia de cadera, identificar componentes implicados en las revisiones y estudiar la duración de los diversos componentes protésicos implantados.
- Objetivos secundarios: Identificar los materiales implantados tras las diversas revisiones, estudiar diversas variables, relacionadas con los pacientes que son sometidos a revisiones de prótesis de cadera, tales como edad, IMC, sexo y conocer el tiempo de ingreso hospitalario precisado.
Materiales y método
Estudio observacional retrospectivo, de 3 años y 8 meses de duración (desde enero 2009 hasta agosto de 2013) que incluyó pacientes sometidos a revisión de artroplastia de cadera en el Hospital Universitario Insular de Gran Canaria.
Población de estudio
- Criterios de inclusión: Pacientes mayores de 14 años, que en el período de estudio hayan sido intervenidos para uno o más recambios de prótesis de cadera por el Servicio de Traumatología y Cirugía Ortopédica del Hospital Universitario Insular y cuyos materiales implantados o sustituidos en las revisiones y motivos de recambio protésico estuvieran recogidos en la historia clínica y ésta fuera accesible.
- Criterios de exclusión: Se excluyeron aquellos pacientes en los que la cronología de los recambios, el tipo de material reemplazado e implantado o el motivo de la sustitución no se especificara en la historia clínica o su registro fuera confuso, y también aquellos pacientes a cuya historia clínica no se pudo tener acceso.
Método
La selección de pacientes se realizó mediante una búsqueda por código en el Libro de Registro de Quirófano del servicio de Traumatología y Cirugía Ortopédica de la Historia Clínica Electrónica (DRAGO®). Dicho código hizo referencia al procedimiento «recambio de prótesis de cadera». La búsqueda se repitió para cada uno de los años estudiados hasta la fecha en curso. Una vez obtenidos los pacientes se procedió a la solicitud de la historia clínica en formato papel y a la revisión de aquellas a las que se pudo acceder.
Variables
- Variables de descripción demográfica: Número de historia clínica, sexo, edad, e Índice de Masa Corporal (IMC).
- Variables relativas a los motivos de intervención: Motivos de recambios protésicos (estableciéndose las siguientes categorías: AA., AS, FP y LUX).
- Variables relativas a los materiales protésicos: Componentes implicados en el recambio protésico: (componentes implicados en AA., AS, FP y LUX), componentes implantados: (Componentes implantados en la primera intervención, componentes implantados en los recambios), y periodo de duración del material protésico.
- Variable relativas al proceso de hospitalización: Periodo de ingreso por cada recambio protésico.
Recogida de datos y análisis estadístico
Los datos de interés se recogieron en un documento del programa Microsoft Word®. Posteriormente, se elaboró una base de datos el en programa Microsoft Excell®, introduciéndose las variables de forma numérica. El análisis estadístico se realizó con el programa informático SPSS V20.0. En los casos donde aplica, todos los test se han desarrollado a dos colas, con un nivel de significación del 5%.
Resultados
Se seleccionaron 40 historias clínicas para el estudio, correspondientes a 18 hombres (45%) y 22 (55%) mujeres, sin embargo, no todos los datos requeridos para el estudio, estuvieron reflejados. La estadística descriptiva de los resultados obtenidos son los indicados las tablas siguientes .
Estuvieron implicados en AS 4 componentes protésicos: cotilo y vástago en un mismo paciente, cabeza femoral y conjunto de toda la prótesis, todos ellos no cementados. Los microorganismos aislados en los cultivos fueron en un caso Staphylococcus epidermidis y Staphylococcus aureus resistente a meticilina y en los otros Staphylococcus epidermidis.
Un único paciente presentó una fractura periprotésica en el tercio superior del fémur y 3 pacientes, luxación de cabeza femoral no cementada. Como sucesivas revisiones se hallaron 6 casos de AA y 8 de LUX .
La variable desconocido hace referencia a pacientes que fueron intervenidos en otro centro, no disponiéndose de datos sobre el modelo protésico que se les implantó originalmente, antes de sufrir un primer AA.
En cuanto la duración del ingreso hospitalario por intervención de revisión de artroplastia de cadera, 13 pacientes (41,94%) estuvieron entre 0 y 9 días ingresados, 16 pacientes (51,61%) entre 10 y 19 días, y 2 pacientes (6,45 %) entre 20 y 29 días. En un segundo ingreso hospitalario para revisión protésica por AA, de 5 pacientes, 4 (80%) estuvieron entre 0 y 9 días hospitalizados y 1 (20%) entre 10 y 19 días. Se presentaron 2 casos de pacientes que estuvieron ingresados por una cuarta revisión debida a un AA y una 6 revisión también debida a un AA respectivamente. Ambos pacientes estuvieron ingresados durante un periodo de tiempo entre 20 y 29 días. Se hallaron 2 pacientes intervenidos por AS en dos tiempos, es ambos casos, el primer ingreso duró entre 10 y 19 días y el segundo, menos de 9 días. Un tercer paciente intervenido por AS, estuvo ingresado menos de 9 días. Por FP, un paciente estuvo ingresado entre 10 y 19 días. Por LUX, 3 pacientes estuvieron entre 10 y 19 días ingresados, y un paciente más de 30 días. Este mismo paciente, estuvo ingresado en una quinta revisión también por luxación entre 20 y 29 días.
Transcurrieron entre 1 y 5 años para 4 pacientes que presentaron una quinta intervención por AA, un AS, y 2 casos de LUX, entre 6 y 10 años transcurrieron para 4 pacientes que presentaron cada uno: una tercera revisión por AA, dos primeras revisiones por AS. y una primera revisión por LUX. El tiempo transcurrido entre una primera revisión y una segunda revisión por AA fue inferior a 1 año para 1 paciente y superior a 20 años para 3 pacientes.
Discusión
A través de este estudio se puede concluir, en cuanto a los motivos que desencadenaron una revisión protésica fueron, en orden de mayor a menor, los siguientes: AA, AS, LUX Y FP.
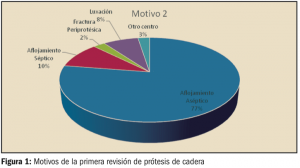
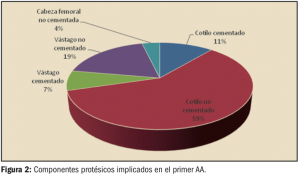
A la vista de los resultados, los componentes no cementados fueron los más frecuentemente implicados en aflojamientos asépticos, concretamente los cotilos no cementados, y en segundo lugar, los vástagos no cementados.
En lo referente a los aflojamientos sépticos, no se puede concluir qué componente estuvo mayoritariamente implicado, sin embargo, en todos los casos se trataron de componentes protésicos no cementados.
Aunque hubo un reducido número de casos de luxaciones, el componente que con más frecuencia se luxó fue la cabeza femoral no cementada.
Los resultados muestran que la mayoría de los pacientes ingresados en el Complejo Hospitalario para revisión protésica fueron intervenidos originariamente para un primer implante en otro centro. La prótesis que con más frecuencia se ha implantado en una primera intervención ha sido el modelo Zweymuller (no cementada) y en las sucesivas revisiones, la prótesis total modelo Solution y los injertos de hueso, han sido los más empleados. En la mayoría de los casos, entre la implantación de la prótesis original y la primera revisión transcurrieron entre 6 y 10 años.
Las mujeres resultaron ser el grupo de pacientes que mayoritariamente fueron intervenidas para revisión protésica. El grupo de edad más afectado, comprende los pacientes entre 61 y 70 años. La mayoría de los pacientes presentaron un IMC correspondiente con «sobrepeso» y en segundo lugar, pacientes clasificables como «obesos» según la clasificación de la OMS. Los días de ingreso requeridos han sido muy variables para cada proceso.
Por último, indicar que en las últimas décadas se han conseguido importantes avances en la cirugía de revisión y en los resultados obtenidos. Una correcta planificación preoperatoria contribuirá a que el cirujano ortopédico realice una artroplastia de revisión de un modo complejo pero previsible. Actualmente se trata de un proceso caro, dificultoso, pero capaz de aportar al paciente un elevado nivel de satisfacción.
|
Tabla 1. Motivos de la primera revisión de prótesis de cadera |
||
|---|---|---|
|
Motivo de la primera revisión |
N |
Porcentaje |
|
Aflojamiento Aséptico (AA) |
31 |
77,5 |
|
Aflojamiento Séptico (AS) |
4 |
10 |
|
Fractura Periprotésica (FP) |
1 |
2,5 |
|
Luxación (LUX) |
3 |
7,5 |
|
Otro centro |
1 |
2,5 |
|
Tabla 2. Componentes protésicos implicados en el primer AA. |
||
|---|---|---|
|
Componentes implicados en 1er AA |
N |
Porcentaje |
|
Cotilo cementado |
3 |
11,11 |
|
Cotilo no cementado |
16 |
59,26 |
|
Vástago cementado |
2 |
7,41 |
|
Vástago no cementado |
5 |
18,52 |
|
Cabeza femoral no cementada |
1 |
3,70 |
|
Tabla 3. Componentes protésicos implicados |
||
|---|---|---|
|
Tipo Componente |
N |
Porcentaje |
|
AA Componente |
48 |
78,69 |
|
AS Componente |
4 |
6,56 |
|
FP Componente |
1 |
1,64 |
|
Lux Componente |
8 |
13,11 |
|
Total |
61 |
100,00 |
|
Tabla 4. Edad de intervención |
||
|---|---|---|
|
AA Edad |
N |
Porcentaje |
|
< 50 |
4 |
11,76 |
|
50 – 60 |
6 |
17,65 |
|
61 – 70 |
13 |
38,24 |
|
71 – 80 |
9 |
26,47 |
|
> 80 |
2 |
5,88 |
|
Tabla 5. Índice de masa corporal En el primer AA. |
||
|---|---|---|
|
AA IMC |
N |
Porcentaje |
|
18,5 – 24,99 |
2 |
14,29 |
|
25,0 – 29,99 |
7 |
50,00 |
|
30,0 – 39,99 |
4 |
28,57 |
|
≥ 40 |
1 |
7,14 |
|
Tabla 6. Prótesis original que sufre AA |
||
|---|---|---|
|
Prótesis original que sufre AA |
N |
Porcentaje |
|
Zweymuller |
6 |
18,75 |
|
Prophor |
4 |
12,50 |
|
Charnley |
1 |
3,12 |
|
Profile |
6 |
18,75 |
|
Thabe Modu |
1 |
3,12 |
|
Corail |
1 |
3,12 |
|
Bicontact |
1 |
3,12 |
|
Versys (no cementada) |
1 |
3,12 |
|
Trilogy |
1 |
3,12 |
|
Deconocido (otro centro) |
10 |
31,25 |
|
Tabla 7. Componentes implantados tras el primer AA. |
||
|---|---|---|
|
AA Modelo implantado |
N |
Porcentaje |
|
Cotilo modelo VerSys |
5 |
8,20 |
|
Polietileno |
5 |
8,20 |
|
Cabeza femoral |
6 |
9,84 |
|
Vástago modelo Revitan |
6 |
9,84 |
|
Total modelo Solution |
9 |
14,75 |
|
Cotilo EP FIT PLUS |
5 |
8,20 |
|
Injerto de hueso |
6 |
9,84 |
|
Cotilo Press Fit |
3 |
4,92 |
|
Vástago Zweymuller |
5 |
8,20 |
|
Otro centro |
1 |
1,64 |
|
Vástago SL-PLUS |
1 |
1,64 |
|
Cerclaje de Dalls Milles |
2 |
3,28 |
|
Cotilo mod no especificado |
4 |
6,56 |
|
Cotilo Revitan |
1 |
1,64 |
|
Cotilo Profile |
1 |
1,64 |
|
Cabeza Femoral Versys |
1 |
1,64 |
|
Tabla 8. Componentes implantados tras un segundo AA. |
||
|---|---|---|
|
2º AA modelo implantado |
N |
Porcentaje |
|
Polietileno |
1 |
11,11 |
|
Total modelo Solution |
1 |
11,11 |
|
Cotilo EP FIT PLUS |
2 |
22,22 |
|
Injerto de hueso |
3 |
33,33 |
|
Cotilo Press Fit |
1 |
11,11 |
|
Vástago SL-Plus |
1 |
11,11 |
|
Tabla 9. Tiempo transcurrido entre el implante protésico inicial y la primera intervención por AA. |
||
|---|---|---|
|
Años entre prótesis original y 1er AA |
N |
Porcentaje |
|
[1 – 5] |
6 |
19,4 |
|
[6 – 10] |
13 |
41,9 |
|
[11 – 20] |
9 |
29 |
|
> 20 |
3 |
9,7 |
Bibliografía
- García García E. Evaluación de la estancia hospitalaria en prótesis de cadera. [Tesis doctoral]. Alcalá. Universidad de Alcalá. Facultad de Medicina; 2011.
- Plaza R, Popescu D, Esteban SG. Fracturas de cadera en las personas mayores de 65 años: diagnóstico y tratamiento. Med Hoy. 5.
- Fractures of the Proximal Femor (Hip) [Internet]. [citado 14 de diciembre de 2013]. http://www.orthoassociates.com/SP11B27/
- Evans PJ, McGgrory BJ. Fractures of the Proximal Fémur. Clinical Review Article. 2012: 30-8.
- Juste Lucero M. Morbimortalidad asociada a la fractura de cadera del paciente anciano. Análisis de nuestro medio. Barcelona. Universidad Autónoma de Barcelona; 2012.
- Corzo J, Marenco JL. Infección de prótesis articular. ¿Cuándo sospecharla? Reum Clínica. 2008; Supl 3:7-12:12.
- Ulrich SD, Seyler TM, Bennett D, Delanois RE, Saleh KJ, Thongtrangan I, Kuskowski M, Cheng EY, Sharkey PF, Parvizi J, Stiehl JB, Mont MA. Total hip arthroplasties: what are the reasons for revision? Int Orthop. 2008; 32(5): 597-604.
- Erens GA, Thornhill TS, Katz JN. Complications of total hip arthroplasty. UpToDate. http://www.uptodate.com/contents/complications-of-total-hip-arthroplasty?source=search_result&search=complications+of+total+hiparthroplasty&selectedTitle=5%7E150#H239249938
- Prokopetz JJ, Losina E, Bliss RL, Wright J, Baron JA, Katz JN. Risk factors for revision of primary total hip arthroplasty: a systematic review. BMC Musculoskelet Disord. 2012; 13: 251.
Plantas medicinales y derivados en el tratamiento de la psoriasis (I): Calaguala
Resumen
Son diversas las especies vegetales que se pueden utilizar para mejorar de forma global al paciente aquejado de psoriasis y para tratar su enfermedad. Entre las plantas de tratamiento destaca la calaguala, pero además se recomiendan plantas depurativas o desintoxicantes como el cardo María, el diente de león o la alcachofera, así como reguladores intestinales tales como las semillas de ispágula, zaragatona o lino; también son de utilidad especies o productos obtenidos de las mismas con propiedades hidratantes, antisépticas o regeneradoras de la piel, como el gel de áloe, el aceite de almendras o diversos aceites esenciales. La calaguala (Polypodium leucotomos) es un helecho que posee propiedades inmunomoduladoras, antioxidantes y fotoprotectoras; además de prevenir los efectos nocivos de la exposición al sol, mejora el vitíligo, melasma, dermatitis atópica, psoriasis y podría ayudar en la pigmentación post-inflamatoria.
La psoriasis es una enfermedad crónica de la piel de carácter inmunológico e inflamatorio, no contagiosa, caracterizada por lesiones distribuidas por todo el cuerpo. Afecta a un 2% de la población (aproximadamente 125 millones de personas en el mundo) y aunque es más frecuente entre los 15 y 35 años de edad, puede desarrollarse a cualquier edad. Puede aparecer de forma repentina o de forma lenta, con remisiones y exacerbaciones de duración muy variable. En ocasiones puede ocasionar una gran discapacidad funcional y psicológica. Por ejemplo, en un estudio reciente se ha comprobado que un 70% de los pacientes considera que su enfermedad incide negativamente en su aspecto físico, condicionando incluso su forma de vestir para disimular las lesiones.
No se conoce con certeza la causa de la enfermedad aunque existen una serie de factores genéticos relacionados con su aparición y desarrollo. Se estima que en un 30 a 40% de los casos existen antecedentes familiares.
También pueden desencadenar un brote de psoriasis o dificultar el tratamiento de un proceso ya instaurado factores externos como agresiones físicas sobre la piel (quemaduras, picaduras de insectos, aire excesivamente seco); factores internos como los de tipo infeccioso bacteriano (faringitis estreptocócica) o viral, administración de fármacos (litio, beta-bloqueantes, interferones) o utilización de drogas de abuso (alcohol), tabaquismo, embarazo, estrés emocional, alteraciones metabólicas (estados de hipocalcemia); y el concurso de alteraciones del sistema inmunológico causadas por enfermedades (artritis reumatoide, SIDA) o tratamientos (quimioterapia).
La propia enfermedad, en sus casos más graves, también puede contribuir al desarrollo de enfermedades como dislipemia, diabetes e hipertensión arterial. Algunas personas con psoriasis, especialmente en el caso de psoriasis ungueal (uñas) presentan mayor riesgo de padecer artritis (artritis psoriásica).
En la mayoría de los enfermos de psoriasis se presentan parches gruesos de color blanco nacarado descamativos (escamas) rodeados de piel rojo-rosada, localizados con más frecuencia en codos, rodillas, cuero cabelludo y parte media del cuerpo. Esto es consecuencia de la reposición excesivamente rápida de las células cutáneas de la piel que se acumulan muertas en la superficie. También son síntomas de psoriasis dolores articulares, alteraciones en las uñas (incremento de grosor, color marrón-amarillento, hoyuelos, desprendimiento de la piel inferior), lesiones genitales en los hombres y excesiva descamación del cuero cabelludo (caspa abundante).
Dependiendo de la extensión de las lesiones se clasifica en leve, moderada o grave y, atendiendo a la localización y características específicas de las lesiones, en cinco tipos principales:
- En placas o vulgar: es la forma más común y frecuente, representa el 80% en adultos y el 75% en niños. Presenta una distribución simétrica en las extremidades (codos, rodillas), zona sacra y cuero cabelludo. Se manifiesta en forma de parches de piel rojos y gruesos recubiertos de escamas blanco-nacaradas.
- Guttata o en gotas, más frecuente en niños y adolescentes. Suele aparecer tras una infección de vías respiratorias altas (Streptococcus pyogenes). Es de aparición brusca en forma de placas pequeñas eritematosas y descamativas por todo el cuerpo.
- Invertida o inversa, se manifiesta en zonas de pliegue como axilas, ingles y zonas inframamarias, perineales, genitales e interglúteas.
- Eritrodérmica, de afectación masiva (90% de la superficie de la piel) en forma de enrojecimiento intenso de la piel. Se trata de una forma grave con riesgo de infecciones y alteraciones hidroelectrolíticas, por lo que requiere cuidados especiales.
- − Pustular: caracterizada por la aparición de pústulas estériles (ampollas blancas llenas de pus) que están rodeadas de piel roja e irritada.
En cualquiera de estas formas es posible la afectación de mucosas. En la mucosa genital aparecen placas eritematosas con o sin descamación, y en la mucosa oral puede producir áreas rojas que cambian de posición en el tiempo.
Para la valoración de la gravedad de la enfermedad se han establecido una serie de escalas normalizadas que también son empleadas en los estudios clínicos realizados para evaluar la eficacia de fármacos de síntesis y productos naturales:
- PSAI (psoriasis área and severity index): índice de área y gravedad de la psoriasis
- BSA (body surface área) área afectada por la enfermedad.
También se emplean escalas de valoración de la calidad de vida como DLQI (dermatology life guality index)
Por lo general se realiza un tratamiento sintomatológico para disminuir el proceso irritativo y prevenir infecciones tanto por vía tópica como sistémica. Se emplean fórmulas de aplicación tópica (cremas o ungüentos) con corticoides, sustancias desescamantes (ácido salicílico), vitamina A o D, baños con avena, etc. También se utiliza la fototerapia sola o en combinación con fármacos fotosensibilizantes.
En casos de psoriasis intensa se emplean por vía oral inhibidores de la respuesta inmunitaria como metrotexato o ciclosporina.
También se pueden aplicar medidas higiénicas que no solo ayuden a mejorar los síntomas sino que puedan prevenir un brote de la enfermedad. Por ejemplo tomar un baño o ducha diaria sin frotarse fuerte para evitar que la irritación de la piel pueda desencadenar un ataque, mantener la piel hidratada, favorecer la exposición al sol pero evitando posibles quemaduras, técnicas de relajación antiestrés, evitar el consumo de alcohol o tabaco.
Son diversas las especies vegetales que se pueden utilizar para mejorar de forma global al paciente aquejado de psoriasis y para tratar su enfermedad. Entre las plantas de tratamiento destaca la conocida vulgarmente como calaguala (Polypodium leucotomos), pero además se recomiendan plantas depurativas o desintoxicantes como puede ser por ejemplo el cardo María, el diente de león o la alcachofera, y reguladores intestinales como las semillas de ispagula, zaragatona o lino.
También son de utilidad especies o productos obtenidos de las mismas con propiedades hidratantes, antisépticas o regeneradoras de la piel, como el gel de áloe, el aceite de almendras o diversos aceites esenciales.
En ocasiones se emplean solas y otras veces de forma conjunta con otros tratamientos. En un trabajo de revisión publicado en 2012 sobre plantas medicinales utilizadas en el tratamiento de la psoriasis, se examinaron los ensayos clínicos publicados en inglés en las bases de datos MEDLINE, EMBASE y CINAHL. En un principio se encontraron 111 artículos incluyendo 63 ensayos clínicos y 28 revisiones. Se seleccionaron finalmente 12 artículos en los que se empleaban plantas medicinales por vía sistémica.
En 4 de ellos se administró oralmente aceites procedentes de plantas más aceites de origen marino. Los otros 8 artículos empleaban formulaciones con diversos ingredientes, siendo en 7, fórmulas de la medicina tradicional China (MTC). En el caso de los aceites, no se puede concluir nada, si acaso algún pequeño beneficio. En los preparados de varias plantas los resultados parecen algo mejores, pero algunos ensayos carecen del rigor necesario y es también difícil llegar a conclusiones válidas. Se aconseja llevar a cabo nuevos ensayos bien diseñados.
Muy recientemente se ha publicado otra revisión sobre plantas de la MTC utilizadas conjuntamente con otra farmacoterapia, en el tratamiento de la psoriasis. Hay que destacar que la MTC se utiliza ampliamente en la psoriasis. Se han revisado las más reconocidas bases de datos y como conclusión las plantas más utilizadas en los estudios revisados son: Rehmannia glutinosa, Salvia miltiorrhiza y Lithospermum erythrorhizon, las cuales han mostrado actividad antiinflamatoria y/o antiproliferativa en estudios experimentales.
Las plantas que se aplican en la psoriasis se recomiendan también, generalmente, para tratar el vitíligo o pérdida crónica de pigmentación en la piel por pérdida sustancial del funcionamiento de los melanocitos epidérmicos. En el vitíligo parecen intervenir factores genéticos y autoinmunes, lesiones neurales o efectos citotóxicos. Igual que ocurre en los pacientes con psoriasis, en muchas ocasiones, estos pacientes ven disminuida su calidad de vida y pueden padecer depresión, ansiedad, pérdida de autoestima, etc.

Calaguala
Polypodium leucotomos Poir., (sin. Phlebodium aureum (L.) J. Smith, Polypodium aureum L.) perteneciente a la familia Polypodiaceae, es un helecho tropical y subtropical originario de América Central y del Sur, conocido entre otros con los nombres vulgares de calaguala, calahuala, polipodio dorado o helecho palma.
El género Polypodium (del griego poly = mucho y podía = pies) comprende un número elevado de especies ampliamente distribuidas, principalmente en zonas subtropicales. En concreto P. leucotomos, es un helecho epífito, rizomatoso, densamente escamoso, con las escamas de color rojizo a dorado. Crece entre 700 y 2500 m de altitud, siendo su óptimo entre 2000 y 2500 m. La especie fue introducida en Europa en el siglo XVIII, al regreso de una expedición del farmacéutico y botánico español Hipólito Ruiz López. Las poblaciones nativas le han atribuido desde hace mucho tiempo propiedades antiinflamatorias y antitumorales; en Europa y en Sudamérica se viene utilizando desde hace años (a partir de los setenta) para tratar afecciones cutáneas como la psoriasis y la dermatitis atópica. Se emplean principalmente los rizomas, pero también las hojas.
El rizoma de calaguala contiene más de un 10% de triterpenos (calagualina), esteroides (ecdisoma, ecdiserona, etc.), lípidos (ácidos grasos poliinsaturados), flavonoides, ácidos fenólicos (p-cumárico, ferúlico, cafeico, 4-OH-cinamoilquínico, clorogénico, etc.), taninos, resina, mucílago y aceite esencial. Se atribuye la actividad principalmente a los compuestos fenólicos, también presentes en las partes aéreas.
Se ha comprobado que diversos extractos preparados a partir de este helecho poseen propiedades antioxidantes, y reducen el daño oxidativo originado por la luz UV, reduciendo la inflamación y la irritación de la piel en modelos animales. Además, las propiedades fotoprotectoras se han demostrado en ensayos in vitro, preservando la capacidad proliferativa de células de piel humanas sometidas a radiación UVA y protegiéndolas de los cambios inducidos por dicha radiación. Esta fotoprotección se debe a su capacidad de inhibir la formación de radicales libres, proteger al ADN y prevenir la muerte celular inducida por la radiación UV.
En un ensayo clínico llevado a cabo durante un año con un número pequeño de voluntarios sanos (10), se ha confirmado el efecto quimiofotoprotector frente a la fototoxicidad inducida por psoraleno-UVA (PUVA, utilizado en el tratamiento de la psoriasis, aunque su uso conlleva riesgos que limitan su empleo). El extracto de calaguala por vía oral, reduce la fototoxicidad, eritema y edema, y el desarrollo subsecuente de hiperpigmentación inducida por PUVA, además protege de forma significativa las células de Langerhans entre otros efectos.
Igualmente se han observado sus propiedades inmunomoduladoras y antiinflamatorias en ensayos in vitro e in vivo. Por otra parte, el extracto acuoso parece ser depresor del SNC, prolongando el tiempo de sueño inducido por pentobarbital, disminuyendo la temperatura corporal y la actividad motora espontánea, etc.
Entre los ensayos clínicos sobre su eficacia en psoriasis, algunos evalúan la eficacia del extracto, otros la comparan frente a placebo, etc. Uno data de 1983 y en él se presenta la experiencia personal del autor, durante dos años, en el tratamiento de la psoriasis con un extracto de calaguala conocido como anapsos. El tiempo medio de los tratamientos fue de seis meses y las dosis administradas diariamente oscilaron entre 80 y 720 mg, dependiendo del peso, edad y fase del tratamiento. Obtuvo buenos resultados en el 61% de los pacientes. Destaca el número elevado de abandonos del tratamiento (119 de 495) que atribuye posiblemente a la lentitud del proceso o a otras causas. Solo se detectaron efectos adversos en dos pacientes, pero desaparecieron al interrumpir el tratamiento. La asociación con radiación PUVA hace que los tratamientos sean mas cortos y parece ser ventajosa.
Un estudio clínico ha evaluado si el extracto de calaguala podría disminuir el uso de corticosteroides tópicos y de antihistamínicos en niños y adolescentes con dermatitis atópica moderada (105 pacientes entre 2 y 17 años de edad). Se trata de un ensayo clínico fase IV, aleatorizado, multicéntrico, doble ciego y controlado frente a placebo. El tratamiento, de seis meses de duración, consistió en la administración por vía oral, de dos cápsulas del medicamento comercializado (240 mg/día de extracto) o placebo, por la noche, a los menores de 6 años. Los niños de entre 6 y 12 años recibieron 360 mg/día de extracto dividido en dos tomas y los mayores de 12 años 480 mg/día de extracto, también dividido en dos tomas. En los brotes se administró metilprednisolona aceponato en emulsión al 0,1%; para la sequedad cutánea, leche hidratante emoliente después del baño; cuando se requirieron corticosteroides sistémicos, se utilizó deflazacort 0,25 a 1,5 mg/kg/día; en caso de prurito, desloratadina en comprimidos o jarabe. El extracto de P. leucotomos fue beneficioso para los pacientes, ya que redujo la necesidad de administrar antihistamínicos y corticosteroides, tanto en cuanto a la duración en días del tratamiento como en cuanto al porcentaje de pacientes. No obstante, la mejoría de la dermatitis atópica fue similar en el grupo tratado y en el placebo.
En un par de revisiones publicadas en 2014 que analizan los ensayos del extracto de P. leucotomos, se concluye que este helecho posee propiedades inmunomoduladoras, antioxidantes y fotoprotectoras. Además de prevenir los efectos nocivos de la exposición al sol, mejora el vitíligo, melasma, dermatitis atópica, psoriasis y podría ayudar en la pigmentación post-inflamatoria. Recientemente se ha comprobado también que minimiza las infecciones en atletas de alto rendimiento. Además su perfil de seguridad es muy elevado. Sería preciso sin embargo, realizar ensayos con mayor tamaño de muestra para confirmar los beneficios.
Los preparados del rizoma están indicados en casos de psoriasis, vitíligo, dermatitis atópica, herpes y problemas inmunológicos. También se puede emplear como fotoprotector tanto por vía tópica como oral, para prevenir el fotoenvejecimiento, las quemaduras solares, tumores de piel y en general en problemas de la pigmentación.
En algunas zonas se emplea para tratar enfermedades neurodegenerativas como la enfermedad de Alzheimer. En este sentido, un ensayo clínico, doble ciego, aleatorizado y controlado frente a placebo sobre 45 pacientes con demencia senil, demostró una mejoría en el rendimiento cognitivo y perfusión sanguínea cerebral tras la administración de 360 mg/día de extracto de calaguala.
En España se encuentra comercializado un extracto de P. leucotomos para ser administrado por vía sistémica; en la ficha técnica de las especialidades figura la siguiente indicación terapéutica: «medicamento a base de plantas indicado para el alivio de los síntomas asociados a procesos inflamatorios leves a moderados de la piel, basado exclusivamente en el uso tradicional». Se presenta en forma de cápsulas conteniendo cada una 120 mg de extracto seco de rizoma de P. leucotomos, correspondiente a 2,5-6,25 mg de ácido quínico.
La posología aconsejada para adultos y adolescentes es: 1 cápsula/3 veces/día, es decir, 360 mg del extracto/día. Esta posología puede aumentarse en una cápsula mas, si es necesario. Los tratamientos deben durar 4 semanas. En niños de 6 a 12 años, siempre previa consulta al facultativo, se recomienda 1 cápsula/2 veces/día, es decir equivalente a 240 mg del extracto/día. No se aconseja en menores de 6 años debido a la falta de estudios de seguridad y eficacia. Tampoco durante el embarazo y lactancia por el mismo motivo.
No se deben administrar antiácidos ni consumir alcohol durante el tratamiento. Precaución en pacientes que toman cardiotónicos ya que puede aumentar sus efectos. Al menos teóricamente, podría también aumentar el efecto de las benzodiacepinas. En raras ocasiones se han manifestado efectos adversos como molestias gástricas, erupción cutánea o prurito.
También se encuentran asociaciones de especies vegetales como por ejemplo, calaguala, pensamiento y bardana, indicada en afecciones de piel y en especial para casos de vitíligo y psoriasis.
Bibliografía
España: Las vacunas como generadoras de ahorro
Los programas de vacunación generan ahorros cinco veces superiores a otras medidas preventivas como la cloración del agua, así como la no inversión en dichos programas se derivan costes económicos, sociales y asistenciales, según el informe El valor económico de la vacunación, ¿por qué la prevención es riqueza?, elaborado por Sanofi Pasteur MSD y presentado en Biospain 2014.
En términos generales, por cada euro invertido en vacunas se ahorran entre 4 ó 5 euros de costes directos (costes relacionados con el tratamiento de las enfermedades que previenen), según el estudio. En el caso de las vacunas infantiles, consideradas en su conjunto (difteria, tétanos, tos ferina, Hib, poliomielitis, sarampión, parotiditis, rubéola y Hepatitis B), el Sistema Nacional de Salud alcanza ahorros superiores a 5 euros en costes directos y a 17 euros en costes indirectos por cada euro invertido en ambos casos.
Igualmente, el estudio señala que la industria de las vacunas contribuye de manera esencial al desarrollo de la economía europea a través de su inversión en I+D y la generación de empleo. El 80% de la producción mundial de vacunas se concentra en Europa, y más del 60% de las fábricas de producción de los 32 principales productores de vacunas se encuentran en la zona euro. En el desarrollo de una vacuna se emplean hasta 33 meses y más de 500 millones de euros.
La elevada especialización e inversión requerida, explica que el mercado de las vacunas cuente con pocos fabricantes. En este especializado y limitado contexto, poder garantizar el suministro de vacunas en un mercado con un incremento constante de la demanda requiere de un marco estable que permita a las compañías fabricantes mantener los niveles de inversión y producción actuales.
España: La industria farmacéutica invirtió 928 millones en I+D en 2013
La industria farmacéutica asentada en España invirtió 928 millones de euros en I+D en 2013, tal y como se desprende de los resultados de la Encuesta sobre Actividades de I+D que elabora cada año Farmaindustria entre sus asociados. Este dato, si bien supone un descenso del 4,6% con respecto al año anterior, consecuencia de los fuertes ajustes sufridos por el mercado farmacéutico, pone de manifiesto que el sector sigue firme en su propósito de liderar las inversiones en I+D industrial de nuestro país, como viene sucediendo en los últimos años.
De estos 928 millones de euros, cabe destacar que 377 millones, es decir alrededor del 41%, se destinaron a contratos de investigación con hospitales, universidades y centros públicos de investigación (lo que se denomina I+D extramuros). Este tipo de investigación es fundamental para el estudio de nuevos fármacos y para el desarrollo científico de estas instituciones y organismos y, desde 2003, la participación de gasto de la industria farmacéutica destinado a este propósito ha aumentado en más de cinco puntos porcentuales.
Por su parte, la investigación interna alcanzó un valor de 550 millones de euros, alrededor del 59% de la inversión total. El mayor porcentaje de estas inversiones se llevó a cabo en Cataluña, casi el 47%, frente al 39 % en Madrid y el 14% que se realizó en otras comunidades o en el extranjero.
En relación al empleo en estas actividades, el sector ocupó a 4.250 personas en 2013. Si bien esta cifra supone un leve descenso respecto a 2012, la cualificación del personal ha aumentado: el 84% de los empleos generados en I+D por la industria farmacéutica corresponde a titulados superiores (licenciados y doctores).
En cuanto a las partidas de gasto invertidas en I+D, la principal –como corresponde a las exigencias actuales de la investigación biomédica- fue la dedicada a ensayos clíni-cos, con algo más de 457 millones de euros. La investigación clínica llevada a cabo por la industria farmacéutica ha aumentado a un ritmo anual del 6% en los últimos 10 años. Por otro lado, la investigación básica, clave para el avance científico, se posicionó en segundo lugar con una inversión de más de 121 millones de euros.
Finalmente, la Encuesta constata el alza de la investigación en biotecnología, ya que el pasado año la industria farmacéutica invirtió 199 millones de euros en este tipo de investigación, lo que supone el 21,5% de la I+D farmacéutica en España.
Argentina: Menos sal, más vida
Este es el título de un programa gubernamental de amplia base destinado a los productores de alimentos y a los consumidores para reducir el consumo de sal y mejorar la salud.
Gracias a la iniciativa “Menos Sal, Más Vida”, los fabricantes de alimentos elaborados de la Argentina están rebajando voluntariamente el contenido en sal de más de 500 productos, los panaderos locales están reduciendo el sodio en el pan, y las familias están prescindiendo del salero en sus comidas.
Al menos el 30% de la población americana padece hipertensión, en gran parte debido al consumo excesivo de sal. Esto tiene como resultado miles de accidentes cerebrovasculares, infartos de miocardio y muertes prematuras, según la Organización Panamericana de la Salud (OPS) y la OMS, que apoyaron decididamente la iniciativa formulando recomendaciones sobre la aplicación de estrategias de reducción de la sal que fueron tomadas en consideración por las autoridades argentinas.
Después de que la Argentina se convirtiera en el segundo país del mundo detrás de Sudáfrica en aprobar un proyecto de ley integral para reducir el consumo de sal, el porcentaje de la población nacional que añade sal a los alimentos tras cocinar o sentarse a la mesa se redujo del 25% en 2009 al 17% en 2013.
El proyecto de ley para reducir el consumo de sal contempla:
La obligación de incluir etiquetas en los alimentos para advertir de los peligros del consumo excesivo de sal.
Limitar el tamaño de los paquetes de sal.
El Ministerio de Salud de la Argentina ha concertado acuerdos voluntarios de reducción de sal con los principales productores de alimentos elaborados del país. En poco tiempo, más de 50 productores clave convinieron en reducir en los años subsiguientes los niveles de sodio en 528 productos, como queso, galletas, pasta, salchichas y sopas, así como en diferentes tipos de pan. El consumo de pan representaba más del 25% del consumo total de sodio en el país.
Internacional: Las desigualdades sociales retrasan el diagnóstico del VIH y su tratamiento
Un estudio elaborado a partir de datos procedentes de seis países europeos relaciona el nivel educativo del paciente con el diagnóstico tardío y con que este tenga lugar en fases más avanzadas de la enfermedad. Incluso en el entorno de Europa occidental, donde son habituales los sistemas de asistencia sanitaria de carácter universal, se producen desigualdades de tipo socioeconómico en el acceso a las pruebas diagnósticas del VIH. Estas son las principales conclusiones de un estudio publicado en la revista AIDS.
Según los autores del estudio, es necesario implementar políticas y realizar intervenciones encaminadas a corregir aquellos determinantes socioeconómicos que producen retrasos en el diagnóstico del VIH y en el inicio de la terapia antirretroviral.
Es ampliamente conocida la existencia de una relación entre tener un nivel socioeconómico bajo y un menor uso del sistema de salud, incluso cuando la asistencia sanitaria es gratuita y accesible. Dada la fuerte asociación entre la epidemia del VIH y los grupos socialmente vulnerables –hombres que tienen sexo con otros hombres (HSH), usuarios de drogas inyectables, inmigrantes (incluidos aquellos en situación irregular)– el efecto del nivel socioeconómico en el diagnóstico y tratamiento de aquellas personas que viven con el VIH cobra una especial relevancia. No obstante, la investigación dirigida al VIH sobre este tema es muy escasa.
Por este motivo, se realizó un estudio de cohortes con datos procedentes de seis países incluidos en la Colaboración de Investigación Epidemiológica Observacional del VIH en Europa (COHERE). Se utilizaron datos de 15.414 personas diagnosticadas con VIH procedentes de Austria, Francia, Grecia, Italia, España y Suiza entre 1996 y 2011. Los resultados analizados en detalle fueron: diagnósticos tardíos de VIH (con un recuento de CD4 inferior a 350 células/mm3), diagnósticos de VIH en fase avanzada (con un recuento de CD4 inferior a 200 células/mm3 y comienzo tardío del tratamiento (recuento de CD4 inferior a 350 células/mm3). Se utilizó el nivel educativo como indicador indirecto de la situación socioeconómica. Concretamente, se tuvo en cuenta el nivel de estudios completados, según la Clasificación Internacional Normalizada (CINE) propuesta por la Organización de las Naciones Unidas para la Educación, la Ciencia y la Cultura (UNESCO). A pesar de que el nivel educativo no representa de forma unívoca la situación socioeconómica, era el único indicador disponible en todos los países del estudio de forma estandarizada. El estudio reflejó un porcentaje general de personas diagnosticadas de forma tardía del 62%, con un recuento de CD4 de 350 células/mm3 o menor. No obstante, la distribución no fue uniforme, dándose el diagnóstico tardío con mucha mayor frecuencia entre aquellas personas que no habían completado estudios primarios (73%) o que habían completado únicamente la educación básica (65%) que entre aquellas con educación secundaria (59%) o superior (55%).
De forma análoga, el porcentaje general de personas con enfermedad avanzada por VIH (recuento de CD4 inferior a 200 células/mm3) en el momento del diagnóstico fue del 40%, dándose una importante variación según el nivel educativo: un 52% en aquellas personas sin estudios primarios, un 45% entre aquellas con estudios básicos, un 37% en aquellas con educación superior y un 31% en las personas que habían completado estudios superiores.
El impacto de la educación en los resultados fue mayor en hombres que en mujeres, especialmente en el caso de HSH. También se apreció un mayor grado de desigualdad en años recientes, lo que resultó más evidente en el caso de Grecia, Italia y España. En lo referente al nivel de células CD4 en el momento del inicio del tratamiento, el valor fue de 173 células/mm3 para las personas sin estudios primarios completados, de 198 células/mm3 para las personas con estudios básicos, de 238 células/mm3 para las personas con educación secundaria y de 251 células/mm3 para las personas con educación superior.
Dicho impacto sería atribuible en gran medida aunque no de forma exclusiva, a un efecto del diagnóstico tardío: aquellas personas que han sido diagnosticadas más tarde empezarán el tratamiento, de forma casi inevitable, también más tarde. Al realizar un análisis solo con aquellos casos que habían sido diagnosticados pronto, se apreció que seguía existiendo una tendencia a un retraso en el inicio del tratamiento entre aquellas personas con menores niveles educativos. Los autores sugirieron posibles explicaciones para las desigualdades identificadas:
La educación es un indicador indirecto del nivel socioeconómico: aquellas personas con mayor nivel educativo tendrían mejores empleos, mejores salarios y más recursos materiales, lo que les permitiría un mejor acceso a los recursos de salud.
La gente con mayor nivel educativo tendría hábitos más saludables, lo que incluye la realización de pruebas del VIH tras haber mantenido conductas de riesgo.
La educación mejora el conocimiento sobre temas de salud, esto incluye aquellas decisiones relativas a la realización de pruebas del VIH y a iniciar a tiempo la terapia antirretroviral, en el caso de ser necesaria.
La educación se relaciona con factores sociales y psicológicos, incluyendo una mayor sensación de control, posición y apoyo social. Aquellas personas con mayor educación tienen que enfrentarse a menos obstáculos para acceder a los cuidados requeridos para tratar la infección por VIH, y son más «resistentes» al estigma que genera.
En el caso de España, según datos del informe de Vigilancia Epidemiológica, del Sistema de Información sobre Nuevos Diagnósticos de VIH, el porcentaje general de diagnósticos tardíos en 2012 fue del 48% y el porcentaje de diagnósticos con enfermedad avanzada fue del 28%. El diagnóstico tardío aumentó con la edad, con un porcentaje del 66% en personas mayores de 49 años. Con relación al mecanismo de transmisión, hubo mayor frecuencia en el grupo de usuarios de drogas inyectadas, llegando al 64%, seguido por heterosexuales (59%) y, con la menor frecuencia, en el grupo de HSH (39%). Estos datos concuerdan con los resultados del presente estudio dado que, a pesar de la existencia de un sistema de salud público y del carácter confidencial de la prueba del VIH, casi la mitad de los diagnósticos de la infección se realizan de forma tardía.
Internacional: La industria farmacéutica mejora la productividad de su investigación
La industria farmacéutica es el sector que más invierte en investigación y desarrollo (I+D) a nivel mundial y, aunque también se han visto afectados por la crisis económica global, están comenzando a resurgir la innovación y la productividad. Así se desprende de un informe elaborado por la consultora KPMG a raíz de una serie de entrevistas a directivos de compañías farmacéuticas, de las que un 58% presentaban ingresos superiores a los 5.000 millones de dólares anuales.
En concreto, los ejecutivos encuestados afirmaron que se está experimentando un resurgimiento de la innovación y solo uno de cada cuatro opinó que la innovación no se está revitalizando en el sector.
Según KPMG en España, el coste estimado de lanzar una nueva entidad química o biológica al mercado se ha más que triplicado, hasta alcanzar los 1.500 millones de dólares; pese a ello, y como aspecto positivo, el número de aprobaciones anuales de nuevos medicamentos por parte de la FDA ha aumentado, lo que se puede considerar como un signo prometedor.
El estudio de KPMG aborda el gran reto de la investigación a ojos de los directivos del sector en el área de I+D, y se analiza la forma de superar las barreras a la innovación.
En este sentido, casi dos tercios de los encuestados aseguran que entre los próximos cinco y diez años al menos la mitad de su presupuesto de I+D se ejecutará externamente, para lo que las empresas también están forjando alianzas más intensas con las universidades: Un fenómeno notable es la tendencia al outsourcing en la I+D, el partenariado y los proyectos de colaboración. Además, según el informe, a nivel mundial se prevé que la suma empleada en la externalización de proyectos para el descubrimiento de nuevos fármacos se duplique hasta alcanzar los 25.000 millones de dólares en 2018.
El informe recuerda que uno de los principales desafíos para la productividad es la gestión de riesgos en inversiones tan elevadas sin restringir la innovación, de ahí que las empresas del sector deban en ocasiones elaborar estrategias para mejorar los esfuerzos de I+D+i a través de la colaboración.
Finalmente, el informe recomienda que el valor del medicamento sea medido en términos de resultados y de mejora de la calidad de vida del paciente, y que ésta sea la guía para la toma de decisiones en todas las fases del ciclo de la investigación farmacéutica.
Coste y eficacia del tratamiento inicial de la infección por VIH en España
A partir de la aparición del primer antirretroviral, para el tratamiento de la infección por el virus de inmunodeficiencia humana (VIH), el panorama sanitario de esta mortal patología en sus inicios ha cambiado drásticamente, convirtiéndose en una patología crónica, prácticamente controlada. La administración de una terapia triple consigue reducir la carga viral plasmática a <50 copias por mL, manteniéndolo durante tiempo. De esta forma, de la mortal enfermedad en los años 80 ha pasado a otra, en donde los pacientes viven prácticamente el mismo tiempo que cualquier persona no infectada. Cabe concluir de lo expuesto que el tratamiento antirretroviral que se recomienda hoy día es muy efectivo; no obstante, ello representa un coste importante a nuestro limitado –presupuestariamente hablando- sistema de salud, por lo que se precisa de un estudio económico que evalúe su eficiencia.
Cada año, el Grupo de Expertos de Sida (GESIDA) en España, indica el tratamiento inicial de pacientes naives (sin tratamiento previo). Entre ellos, algunos se han considerado como preferentes por la totalidad del grupo y el Plan Nacional sobre el SIDA, como TDF/FTC/EFV y TDF/FTC más ATV/r, DRV/r o RAL (siendo: TDF: tenofovir; FTC: emtricitabina; EFV: efavirenz; ATV: atazanavir; r: potenciado con ritonavir; DRV: darunavir y RAL: raltegravir).
Para el estudio, los autores3 diseñaron un árbol de decisión que simula la evolución de cada tratamiento analizado, respecto de la eficacia mostrada, los efectos adversos observados y los abandonos producidos, todos ellos a partir de los ensayos clínicos efectuados. En dicho modelo, los pacientes entran al inicio de cada tratamiento, en cuyo caso pueden finalizar el mismo –mostrando la consecución o no del éxito terapéutico- o abandonar por diversas causas (efectos adversos, fallo virológico, pérdida del paciente, no adherencia al tratamiento, embarazo, muerte u otros). El horizonte temporal analizado es de 48 meses.
El beneficio analizado, la eficacia, se midió mediante la tasa de respuesta, considerando ésta como la consecución de una carga viral indetectable de menos de 50 copias por mL en la semana 48 desde el inicio del tratamiento.
Dada la perspectiva del análisis, del sistema nacional de salud, se incluyeron sólo los costes sanitarios directos que fueran diferenciales en las diferentes alternativas, a saber, tratamiento antirretroviral, manejo de los efectos adversos, estudio genotípico de resistencias y determinación de HLA B*5701.
Los resultados obtenidos deben analizarse con cautela pues se expresaron en el coste necesario para conseguir un paciente con respuesta terapéutica a los 48 meses, en vez de estimar el coste incremental de obtener un paciente adicional con respuesta de una alternativa terapéutica más costosa respecto de otra –para analizar la eficiencia relativa de uno respecto de otro. En ese caso, se podría estimar si una terapéutica más eficaz pero también más costosa supone o no una adecuada asignación de los recursos.
Los datos de resultados, en el caso base, se describen en la Tabla 3.
Con los resultados obtenidos, los autores concluyen que, considerando el precio oficial de los tratamientos antirretrovirales, la pauta TDF/FCT/RPV presenta el menor ratio de coste por paciente con respuesta terapéutica.
|
Tabla 3 |
|||
|---|---|---|---|
|
|
Coste (€) |
Eficacia |
Coste/eficacia |
|
TDF/FCT/EFV (*) |
7.651 |
0,8 |
9.556 |
|
ABC/3TC + EFV |
6.894 |
0,68 |
10.135 |
|
TDF/FTC/RPV |
6.965 |
0,83 |
8,396 |
|
TDF/FTC + NPV |
6,747 |
0,73 |
9,218 |
|
TDF/FTC +ATV/r (*) |
9,660 |
0,79 |
12,155 |
|
TDF/FTC + DRV/r (*) |
9,619 |
0,84 |
11,456 |
|
TDF/FTC + LPV/r |
9,025 |
0,75 |
12,092 |
|
ABC/3TC + ATV/r |
8,891 |
0,66 |
13,512 |
|
ABC/3TC + LPV/r |
8,419 |
0,66 |
12,718 |
|
TDF/FTC + RAL (*) |
12,059 |
0,87 |
13,930 |
|
ABC/3TC + RAL |
11,413 |
0,87 |
13,181 |
(TDF: tenofovir; FTC: emtricitabina; EFV: efavirenz; ABC: abacavir; 3TC: lamivudina; RPV: rilpivirina;
NPV: nevirapina; ATV: atazanavir; r: potenciado con ritonavir; DRV: darunavir ; LPV: lopinavir y RAL:
raltegravir); (*) pauta preferente de tratamiento
