Información de seguridad procedente de la evaluación periódica de los datos de farmacovigilancia que decide el PRAC
 Nº449
Nº449
El Comité europeo para la Evaluación de Riesgos en Farmacovigilancia (PRAC) ha acordado cambios en la información autorizada de las fichas técnicas y de los prospectos de los medicamentos europeos por motivos de seguridad. Una vez que se revisan y evalúan los datos de los informes periódicos de seguridad (IPS; en inglés, PSUR) de forma colaboradora entre las 27 agencias nacionales, se presentan los cambios y se acuerdan en las reuniones mensuales del PRAC. A continuación, se muestran los últimos cambios de información de seguridad acordados recientemente en el PRAC.
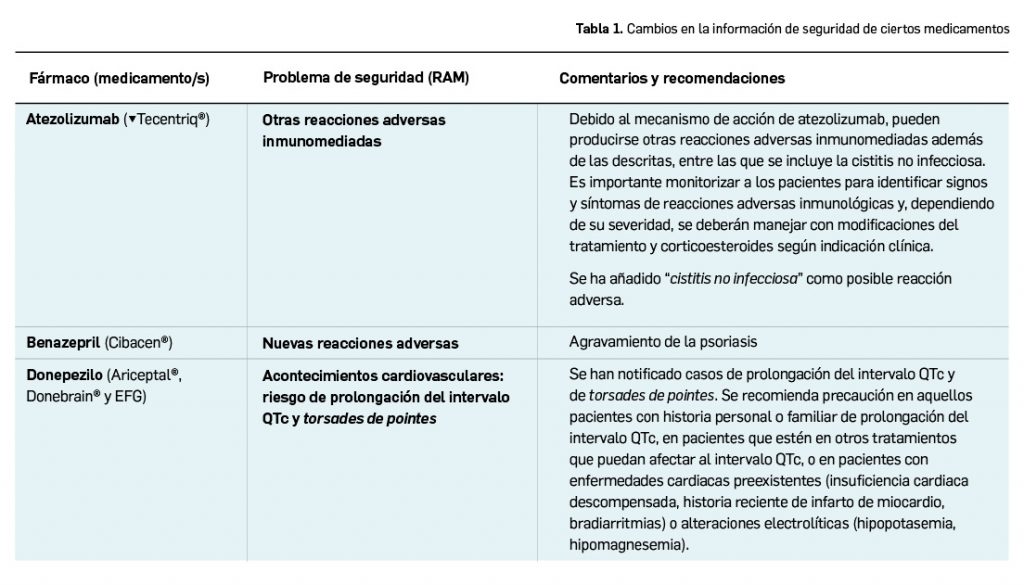
El Comité europeo para la Evaluación de Riesgos en Farmacovigilancia (PRAC) ha acordado cambios en las fichas técnicas y los prospectos de los siguientes medicamentos, siendo los más importantes los que se describen en la Tabla 1, según informa la AEMPS en su Boletín de Seguridad de Medicamentos de Uso humano de julio de 2021. Las fichas técnicas y prospectos de los medicamentos pueden consultarse en la web de la AEMPS, dentro de la sección del Centro de Información Online de Medicamentos – CIMA, disponible en: https://cima.aemps.es/cima/publico/home.html.
Bibliografía
-
- Agencia Española de Medicamentos y Productos Sanitarios. Nueva información de seguridad procedente de la evaluación periódica de los datos de farmacovigilancia. Boletín mensual de seguridad de la AEMPS sobre medicamentos de uso humano del mes de julio de 2021. Disponible en: https://www.aemps.gob.es/informa/boletines-aemps/boletin-fv/2021-boletin-fv/boletin-mensual-de-seguridad-de-la-aemps-sobre-medicamentos-de-uso-humano-del-mes-de-julio-de-2021/ (acceso a 30 de noviembre de 2021).




