Condrocitos autólogos en lesiones del cartílago de la rodilla
 Nº472
Nº472
Resumen
CEMTROCELL es un nuevo medicamento de terapia avanzada –producto de ingeniería tisular – cuyo principio activo son condrocitos adultos diferenciados autólogos, obtenidos a partir de una biopsia de cartílago articular y expandidos ex vivo, para los que se ha postulado que, una vez distribuidos sobre la membrana de colágeno y colocados sobre la lesión del cartílago, promueven la proliferación y diferenciación de las células cultivadas, probablemente originando la síntesis de tejido de reparación cartilaginoso de tipo hialino. En base a ello, el medicamento, que será elaborado de forma individualizada, se ha autorizado para su uso exclusivo en la Clínica CEMTRO de Madrid para la reparación –en un procedimiento quirúrgico de implantación intraarticular– de lesiones sintomáticas del cartílago de la rodilla (grado III o IV de la ICRS) en pacientes adultos. Se contraindica en pacientes con artrosis avanzada de rodilla o en quienes el fémur aún esté en crecimiento.
La evaluación de su eficacia se ha llevado a cabo a partir de la experiencia clínica en la Clínica CEMTRO, con datos de 83 pacientes adultos de mediana edad, en su mayoría con lesiones únicas del cóndilo o de la rótula, de superficie mediana de 4 cm2 y afectación superior al 50 % del grosor del cartílago. Tomando como referencia el periodo de seguimiento de 2 años desde la administración, se ha visto que el medicamento reduce notablemente el dolor asociado a la lesión; también mejora de forma relevante la funcionalidad de la articulación y se asocia con un mejor patrón radiológico, indicativo de reparación del cartílago.
Asimismo, su perfil de seguridad parece encontrarse en la línea de tratamientos similares de implantación de condrocitos autólogos. Las principales reacciones adversas que se notifican en relación con el procedimiento quirúrgico de administración intraarticular son: inflamación, dolor o fibrosis de la articulación, menor amplitud de movimiento y pirexia; estas son en general leves y desaparecen con el paso del tiempo. En los 2 primeros años de seguimiento, solo un paciente había notificado eventos adversos relacionados con el medicamento, 2 a los 3 años y 1 a los 5 años: se describen como reacciones adversas el fracaso del tratamiento y la delaminación.
En ausencia de comparaciones directas con otras estrategias terapéuticas usadas en este contexto clínico, especialmente Spherox®, no se pueden sacar conclusiones claras sobre el posicionamiento de este nuevo fármaco. Su carácter de tratamiento unicéntrico y el hecho de que las variables de eficacia empleadas difieren parcialmente de las investigadas con otras terapias avanzadas aprobadas hasta la fecha en indicaciones similares impiden la realización de comparaciones indirectas. A la vista de la bibliografía existente y habida cuenta del tipo de tratamiento, CEMTROCELL parece representar una alternativa interesante –aunque con un procedimiento más complejo– frente a la microfractura en el manejo de lesiones pequeñas de cartílago (< 4 cm2), sobre todo si son lesiones recientes. Puede mejorar la sintomatología y funcionalidad de la rodilla, pero, en cualquier caso, no representa una cura y la eficacia a largo plazo de las terapias a base de condrocitos autólogos ha sido puesta en entredicho, como en el caso del parecido ChondroCelect®, por lo que es necesario disponer de datos de mayor calidad y con mayor seguimiento para concluir sobre el beneficio clínico que realmente aporta CEMTROCELL.
Introducción
En términos generales, la autorización de comercialización de los medicamentos de terapia avanzada (MTA) se realiza mediante el procedimiento centralizado que dicta la Directiva 2001/83/CE del Parlamento Europeo y del Consejo, de 6 de noviembre de 2001. Sin embargo, el Reglamento (CE) Nº 1394/2007, sobre medicamentos de terapia avanzada, contempla la exclusión de algunos de estos medicamentos del procedimiento centralizado de autorización si se fabrican en un hospital a medida para un solo paciente con prescripción facultativa y sujetos a normas de calidad específicas. Es lo que se conoce como “cláusula de exención hospitalaria”1, cuya competencia de concesión corresponde a las autoridades nacionales (en España, a la AEMPS), que exigen unas normas de fabricación equivalentes a las de los medicamentos industriales, así como datos de seguridad y eficacia.
Al amparo de lo estipulado a nivel estatal en el Real Decreto 477/20142, de 13 de junio, por el que se regula la autorización de medicamentos de terapia avanzada de fabricación no industrial, la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) autorizó el pasado 31 de octubre de 2023 el medicamento “CEMTROCELL 50.000 células/microlitro – Suspención para implantación”, aprobando para él una ficha técnica y prospecto, como tienen el resto de los medicamentos.
Desarrollado por la Clínica CEMTRO de Madrid, se trata del tercer medicamento de terapia avanzada de fabricación no industrial –entre la comunidad biomédica, también se les conoce coloquialmente como medicamentos académicos o terapias avanzadas académicas– que recibe una autorización de uso por parte de la AEMPS, tras el medicamento NC1 del Hospital Universitario Puerta de Hierro de Majadahonda y el ARI-0001 del Hospital Clínic de Barcelona, que fueron autorizados, respectivamente, en 2019 para el tratamiento de lesiones medulares traumáticas y en 2021 frente a casos en recaída y refractariedad de leucemia linfoblástica aguda de células B CD19+ (Fernández-Moriano, 2020; Fernández-Moriano, 2021).
Este tipo de autorización de uso (AU) presenta ciertas características diferentes a las autorizaciones de comercialización comúnmente concedidas a los medicamentos de fabricación industrial, pues habilita a la producción y administración del medicamento exclusivamente a un hospital en concreto (se trata de un medicamento calificado como de Uso Hospitalario por la AEMPS), responsable del tratamiento y el único centro que por ahora podrá llevarla a cabo. No obstante, conviene recordar que el procedimiento para la solicitud de una AU no es diferente a la presentación de cualquier otro dossier para la autorización de un medicamento, debiendo acreditar, con las especificidades propias de las terapias avanzadas, los datos preclínicos, clínicos y de calidad suficientes para evaluar el balance beneficio/riesgo positivo.
Las AU contienen generalmente elementos de condicionalidad (se conceden por 3 años y son revisables) que obligan y comprometen a su titular a continuar con la investigación clínica –y presentar un informe anual– para mantenerla, igual que ocurre con el resto de las terapias avanzadas a nivel de la UE, por lo que podría considerarse como un proceso similar a una autorización condicional por procedimiento centralizado. Tiene, por tanto, un doble objetivo: permitir el acceso a pacientes que no tienen otras alternativas de tratamiento y continuar generando conocimiento sobre el medicamento hasta que, eventualmente, consiga una autorización de comercialización centralizada para toda la UE.
Aspectos fisiopatológicos
Las lesiones del cartílago de la rodilla, también llamadas condrales u osteocondrales, ya sean de naturaleza aguda o crónica, que se producen como consecuencia de una sobrecompresión del tejido cartilaginoso o de cizallamiento a nivel subcondral, suelen acabar en un proceso degenerativo.
En las personas mayores esta degeneración del cartílago articular requiere inevitablemente la sustitución total de la articulación por una prótesis artificial; afortunadamente, sin embargo, en los pacientes jóvenes este tipo lesiones cartilaginosas pueden ser solucionados o reparadas antes de que se transformen en un cuadro degenerativo abierto.
El posible origen de las lesiones condrales es diverso, aunque las causas más frecuentes son las debidas a traumatismos directos o por torsión, así como a una osteocondritis disecante. Las lesiones de origen traumático consisten en fisuras, colgajos condrales o desgarros, o en la pérdida de un segmento de cartílago articular, pudiendo presentarse de manera aislada o junto a otras lesiones articulares, como rotura del ligamento cruzado anterior, especialmente en deportistas. Aunque sobre la rodilla pueden actuar diferentes fuerzas, la mayoría de las lesiones ocurren por fuerzas de cizallamiento; por su parte, la osteocondritis disecante puede ser el resultado de la insuficiente o inadecuada consolidación de una fractura osteocondral. En este sentido, lo que se conoce como laminación consiste en la separación del cartílago del hueso subcondral por dichas fuerzas de cizallamiento.
Básicamente, pueden producirse tres tipos de lesiones a nivel del cartílago de la rodilla:
- Alteraciones de las células y la matriz extracelular sin lesión macroscópica de la superficie articular.
- Lesión macroscópica del cartílago articular sin afectación del hueso subcondral.
- Lesión macroscópica del cartílago articular y el hueso subcondral subyacente: fractura osteocondral.
Las lesiones microscópicas del cartílago articular pueden ser debidas a un traumatismo único o a microtraumatismos repetidos. Independientemente de la causa, se observan bandas de condrocitos muertos que dificultan los procesos de degradación y síntesis de la matriz extracelular. Como consecuencia de esto último, hay una disminución de proteoglicanos y una desorganización ultraestructural del colágeno y un aumento de la hidratación tisular. Estos cambios provocan un aumento de la permeabilidad y una disminución de su rigidez.
Las lesiones condrales abarcan la capa cartilaginosa más blanda y suelen localizarse en el cóndilo femoral lateral y en la superficie medial de la rótula. Estas lesiones aparecen habitualmente en personas en las que su esqueleto ha completado su madurez, mientras que las fracturas osteocondrales afectan habitualmente a pacientes con esqueleto inmaduro.
En las lesiones condrales traumáticas, se pueden apreciar en las zonas en que se ha producido el impacto daños macroscópicos del cartílago, generalmente consistentes en fisuras o fragmentos desprendidos, pero que raramente afectan al hueso subcondral. Tales lesiones no suelen ocasionar hemorragia intraarticular ni respuesta inflamatoria, ya que el tejido cartilaginoso carece de vasos sanguíneos. Aunque los condrocitos responden sintetizando matriz, no lo hacen en cantidad insuficiente para reparar todo el defecto, lo que implica que la capacidad de cicatrización espontánea del cartílago articular es mínima; por el contrario, las lesiones cartilaginosas inducen una destrucción progresiva de la superficie articular.
Además, las citocinas, péptidos y componentes macromoleculares del líquido sinovial pueden potenciar la lesión del cartílago. En definitiva, aunque el daño queda limitado al cartílago articular durante los estadios iniciales, la evolución subsiguiente de la lesión implica la afectación del hueso subcondral y de las estructuras óseas de la epífisis.
La clasificación más usada para describir las lesiones condrales es la Clasificación modificada de la Sociedad Internacional de Reparación del Cartílago (ICRS, por sus siglas en inglés), que incluye 5 grados, de menor a mayor nivel de afectación:
- Grado 0: cartílago articular normal.
- Grado I: reblandecimiento y tumefacción del cartílago articular en un área irregular, con lesiones superficiales.
- Grado II: fragmentación y fisuración de menos del 50 % de profundidad del cartílago.
- Grado III: la fragmentación y fisuración se extienden hasta el área del hueso subcondral, habiendo presencia de defectos cartilaginosos en más del 50 % del grosor, pero sin llegar a atravesar hueso subcondral.
- Grado IV: hay exposición del hueso subcondral, lo que implica ulceración o incluso pérdida completa del cartílago.
En la fractura osteocondral, a diferencia de la que está limitada solo al cartílago, se produce hemorragia y formación de coágulo de fibrina, lo que activa la respuesta inflamatoria con alteración del líquido sinovial. Esta reacción inflamatoria y el coágulo de fibrina se extienden sobre la superficie articular afectada, y las plaquetas presentes liberan factores mediadores vasoactivos y factores de crecimiento y otras citocinas. Dado que hay compromiso óseo, la matriz extracelular participa a este nivel y contribuye de manera importante a la curación, estimulando la invasión vascular y la migración de células indiferenciadas que evolucionarán a condrocitos con todas sus capacidades funcionales. Por su parte, en la parte ósea de la lesión se genera tejido óseo inmaduro que posteriormente se transformará en maduro. Al final se produce un tejido cartilaginoso estructuralmente similar al normal, pero que con el paso del tiempo va perdiendo condrocitos y proteoglicanos y la matriz extracelular acaba consistiendo en colágeno tipo I. Generalmente a lo largo del primer año tras la lesión, especialmente si es grande, este tejido se desintegra dejando expuestas zonas de hueso subcondral.
En cualquier caso, la imposibilidad del cartílago para reparar sus propias lesiones hace que el tratamiento de las pérdidas focales del cartílago no esté resuelto definitivamente.
La artroscopia es considerada como el mejor método para confirmar el diagnóstico, así como la localización y el tipo de lesión, permitiendo además instaurar una corrección quirúrgica en el mismo acto. Se han propuesto diversas técnicas quirúrgicas para tratar los defectos condrales, incluyendo técnicas de reparación, como lavado artroscópico o estimulación del hueso subcondral y técnicas de regeneración como aloinjertos osteocondrales, injerto osteocondral autólogo (mosaicoplastia), implantación de condrocitos autólogos cultivados y el implante de fibras de carbón, basado en su capacidad para inducir la formación de colagenasa y una reacción fibrosa que cubra el daño condral. En las pequeñas lesiones o defectos del cartílago articular (< 4 cm2, sin eficacia en lesiones de mayor extensión) se suele utilizar con buenos resultados la técnica de la microfractura, que consiste en practicar una incisión en el hueso subcondral provocando la consiguiente hemorragia, lo que es capaz de inducir la formación de un coágulo de fibrina y estimular la formación de fibrocartílago, resultando todo ello en mejorías funcionales de la articulación (Cuéllar, 2013).
Entre las alternativas farmacológicas más recientes, destaca la comercialización entre 2009 y 2016 (retirado a instancias del laboratorio titular por motivos comerciales) del primer medicamento de terapia avanzada, ChondroCelect®, considerado un medicamento de ingeniería tisular que consistía en una suspensión de condrocitos autólogos3 (del propio paciente), viables y caracterizados, cultivados ex vivo, que expresan marcadores proteicos específicos. Estaba indicado para la reparación de lesiones sintomáticas únicas del cartílago del cóndilo femoral de la rodilla (grado III o IV de la clasificación ICRS) en adultos, pudiendo existir lesiones cartilaginosas asintomáticas concomitantes (grado I o II de la ICRS).
La demostración de eficacia se basó en los resultados de un ensayo clínico pivotal de fase 3, controlado (con el procedimiento de microfractura para reparación de lesiones sintomáticas únicas del cartílago de los cóndilos femorales de la rodilla), aleatorizado y multicéntrico, en pacientes adultos (18-50 años) con lesiones de entre 1 y 5 cm2, en el que, tras la administración de los condrocitos4, se cerró la superficie con periostio y se selló con cola de fibrina, si bien para futuras aplicaciones se valoraba cubrir el defecto mediante una membrana de colágeno biodegradable.
Tal como recogía la ficha técnica, los resultados de la exploración histológica de la biopsia a los 12 meses del tratamiento indicaron una reparación estructural superior en el grupo del medicamento (n= 51) en comparación con el control (n= 61). Hubo una mejora continua de hasta 36 meses en la medida de la variable clínica KOOS5 (puntuación en la escala de valoración de la artrosis y las lesiones de rodilla, Knee Injury and Osteoarthritis Outcome Score) en los 2 grupos de tratamiento, siendo el beneficio estimado mayor con ChondroCelect®, pero sin alcanzar significación estadística. Los pacientes que hacía menos de 3 años que presentaban síntomas fueron quienes más se beneficiaron del medicamento, no viéndose diferencias significativas entre grupos en los pacientes con mayor duración de las manifestaciones. El seguimiento de los pacientes a más largo plazo (5 años) permitió confirmar el efecto de los tratamientos, pero no se vieron diferencias estadísticamente significativas de los beneficios clínicos entre el grupo de ChondroCelect® y el de microfractura en la población global, sino solo en el subgrupo de pacientes con aparición reciente (< 3 años) de los síntomas.
Los datos de seguridad obtenidos en estos pacientes no indican ningún problema específico y confirman una incidencia de hipertrofia menor. Se observaron reacciones adversas en el 78 % de los pacientes durante un periodo de seguimiento postoperatorio de 36 meses. Entre las reacciones adversas más frecuentes o graves relacionadas con el medicamento se observaron artralgia, hipertrofia del cartílago, crepitación articular, derrame sinovial, fracaso del tratamiento o deslaminación. Las reacciones adversas –esperables– relacionadas con la intervención quirúrgica incluían inflamación articular (postoperatoria), artralgia, pirexia, artrofibrosis o menor amplitud de movimiento de la rodilla; fueron en su mayoría leves y desaparecieron en las semanas siguientes a la cirugía.
Otro medicamento de ingeniería tisular similar, autorizado en 2013 en la UE (pero suspendido desde 2014 –y después retirado definitivamente– por el cierre del lugar de fabricación por decisión comercial del laboratorio), ha sido MACI®, acrónimo del inglés matrix applied characterised autologous cultured chondrocytes, que hace referencia a que el principio activo del medicamento eran condrocitos autólogos viables caracterizados, cultivados ex vivo, que expresan marcadores específicos de condrocitos y van sembrados en una membrana de colágeno de tipo I/III (de 14,5 cm2) de origen porcino con marcado CE; cada implante contenía entre 500 000 y 1 millón de células/cm2 de membrana, a recortar por el cirujano según la medida y la forma de la lesión, asegurando que la zona afectada queda cubierta con las células hacia abajo. Se indicaba para la reparación de lesiones sintomáticas completas del cartílago de la rodilla (grado III o IV de la escala modificada de Outerbridge) de 3 a 20 cm2 de extensión en pacientes adultos con esqueleto maduro.
Su aprobación se sustentó en los resultados de un ensayo clínico pivotal aleatorizado, controlado (con microfractura), abierto y de grupos paralelos (SUMMIT2), en que participaron 144 pacientes adultos (media de edad de 35 años) con lesiones focales del cartílago de la rodilla de una mediana de 4 cm2 (rango 3-20) y grado III-IV según la clasificación de Outerbridge, por lo general pretratados con cirugías ortopédicas de rodilla. El medicamento se mostró significativamente superior a la microfractura: hubo una mejora clínica y estadísticamente relevante desde el estado basal hasta la semana 104 tanto en la escala KOOS de funcionalidad como en el dolor en los pacientes tratados con MACI® sobre el comparador (p= 0,001). Sin embargo, no se vieron diferencias reseñables respecto a la reparación estructural del cartílago hialino (relleno de la lesión evaluado por resonancia magnética) ni a la calidad del tejido de reparación (evaluado mediante análisis histológico).
El perfil de seguridad de MACI® se relacionó fundamentalmente con complicaciones del procedimiento de la propia cirugía (como trombosis venosa profunda y embolismo pulmonar), de otras patologías de la rodilla (de ligamentos o de menisco) o de la extracción de la biopsia. Entre las complicaciones asociadas con el propio implante se han descrito hipertrofia sintomática del injerto y delaminación del injerto (total o parcial, posiblemente dando lugar a cuerpos libres en la articulación o a un fracaso del injerto).
Por último, es preciso citar al único medicamento de ingeniería tisular hoy en día disponible en la UE –autorizado en 2017, aunque se comercializaba previamente en ciertos países (incluido España)– para la indicación en adultos de reparación de lesiones sintomáticas del cartílago articular de la rodilla –cóndilo femoral y rótula– de grado III o IV de la ICRS y tamaño de < 10 cm2: Spherox®. El medicamento consiste en una suspensión en solución isotónica de NaCl de agregados esféricos (esferoides) de condrocitos autólogos humanos cultivados ex vivo6 y unidos a una matriz para su implantación intraarticular. Cada jeringa precargada contiene un número especifico de esferoides que depende del tamaño de la lesión a tratar, y también debe ser administrado por procedimiento quirúrgico (preferiblemente artroscopia o mini-artrotomía) en un centro sanitario.
Tras probarse en modelos animales que no parece haber riesgos derivados del uso de esferoides en humanos, su autorización se basó en los hallazgos de un estudio de fase 2, multicéntrico, aleatorizado, no controlado (la microfractura no se recomienda en lesiones extensas) y abierto, en el que participaron 75 pacientes adultos (media de 34 años) con lesiones condrales focalizadas (grado III o IV de la ICRS y superficie afectada de 4-10 cm2), quienes recibieron distinta cantidad de esferoides por grupos. Los cambios observados en cada uno de los tres niveles de dosis evaluados fueron similares y en todos se observó una mejoría significativa (p< 0,05) en la puntuación de KOOS en comparación con el estado basal: el análisis combinado reveló un aumento desde un promedio de 57 puntos hasta 73, 75 y 77 puntos tras 12, 24 y 36 meses, respectivamente. Las medidas con otras escalas validadas, incluida la IKDC (subjetiva), mostraron resultados consistentes con los anteriores. Incluso las investigaciones por resonancia magnética indicaron una mejora en los primeros 3 años después del tratamiento (aumento de puntuación según el sistema MOCART, Magnetic Resonance Observation of Cartilage Repair Tissue).
Posteriormente, se han hecho públicos los resultados de un ensayo clínico de fase 3, también multicéntrico y aleatorizado, pero controlado (con microfractura), que incluyó a 102 pacientes adultos (37 años de edad media, 60 % mujeres) con lesiones condrales de 1 a 4 cm2 de extensión en el cóndilo femoral de la rodilla sin pretatar. Se hizo el seguimiento de los pacientes durante 5 años posteriores a la administración y se vio que, en ese punto final, con Spherox® se producía un aumento de entre 22 y 28 puntos (desde un basal de 57 puntos) en la escala KOOS, mostrándose el nuevo medicamento con una eficacia similar al procedimiento de la microfractura (Hoburg et al., 2022).
Desde el punto de vista de la seguridad, los eventos adversos más importantes que se han comunicado son los esperados tras la intervención, y comparables con tratamientos similares: se han registrado casos limitados o únicos de trombosis venosa, embolia pulmonar, retraso en la curación de la lesión, edema de médula ósea, y bloqueo doloroso, derrame e inflamación de la articulación; también se ha descrito un riesgo de delaminación e hipertrofia del trasplante, así como de falta de eficacia a causa de la delaminación. Los datos poscomercialización no han proporcionado ninguna señal de preocupación adicional, si bien el medicamento no debe usarse en pacientes con osteoartritis, con crecimiento óseo activo o con infecciones por virus de hepatitis B o C o VIH.
Acción y mecanismo
CEMTROCELL es un nuevo medicamento de terapia avanzada –producto de ingeniería tisular1– cuyo principio activo son condrocitos diferenciados adultos autólogos, obtenidos a partir de una biopsia de cartílago articular y expandidos ex vivo. Aunque no se han realizado estudios farmacodinámicos convencionales en su desarrollo, las pruebas clínicas y no clínicas desarrolladas con anterioridad con medicamentos similares sugieren que la distribución de condrocitos autólogos sobre la membrana de colágeno y su colocación sobre la lesión del cartílago articular promueve la proliferación y la nueva diferenciación de las células cultivadas y puede dar lugar a la síntesis de tejido de reparación cartilaginoso de tipo hialino.
El medicamento ha sido aprobado para su uso por vía intraarticular para la reparación de lesiones sintomáticas del cartílago de la rodilla (grado III o IV de la ICRS) en pacientes adultos. El medicamento se implanta localmente en un procedimiento quirúrgico que debe ser realizado en condiciones estériles por un cirujano específicamente entrenado y cualificado en el uso de CEMTROCELL. Dado su carácter autólogo, el medicamento es elaborado y utilizado individualmente en cada paciente, teniendo en cuenta que la cantidad de células a implantar depende del tamaño de la lesión del cartílago (la dosis recomendada de 5 millones de células/cm2).
El procedimiento de implantación de condrocitos autólogos (ICA) requiere la realización de una incisión para dejar expuesta la lesión, tras lo cual el tejido cicatricial enfermo se cruenta y desbrida hasta llegar al hueso subcondral sano y al cartílago sano circundante. Allí se marca la lesión con rotulador quirúrgico que va a servir para tomar la medida en un molde estéril, usando como transportador una membrana de colágeno I/III. A continuación, se corta la membrana seca del tamaño y forma de la lesión y se siembran las células en la membrana en la cara rugosa a la dosis celular requerida, quedando dispuestas entre las fibras de colágeno (una vez adsorbidas a la membrana, proceso que tarda unos 12 minutos). Después, la membrana se coloca sobre la lesión y se sutura al cartílago sano próximo, sellando entre los puntos con pegamento de fibrina y comprobando la estabilidad de la membrana mediante la movilización de la articulación. El fin de ese paso es asegurar la retención de los condrocitos implantados en la zona lesionada y su contacto directo con el lecho defectuoso. Finalmente, se realiza el cierre por planos de la articulación y se coloca un vendaje compresivo. La implantación debe ir seguida de un programa de rehabilitación adecuado durante aproximadamente un año (AEMPS, 2022).
Aspectos celulares
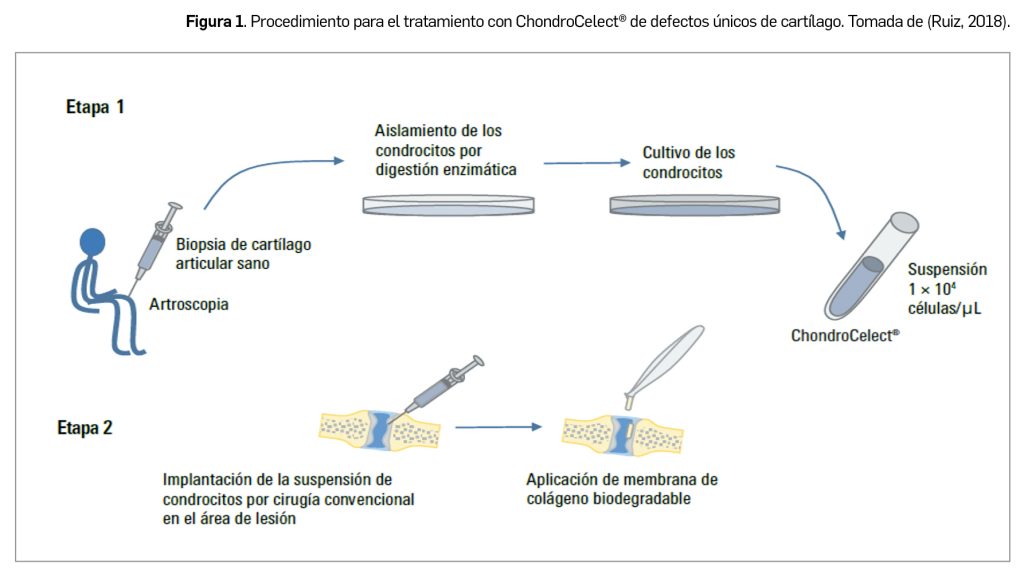
Según se ha indicado, CEMTROCELL es una terapia avanzada a base de condrocitos adultos obtenidos de una biopsia tomada –por artroscopia– de una zona sana del cartílago del propio paciente, de donde se aíslan las células y se cultivan posteriormente en laboratorio. En la primera se obtiene una biopsia del cartílago sano de la rodilla del paciente mediante artroscopia, lo que permite el aislamiento, cultivo y ampliación de condrocitos sanos. Las células obtenidas en esta etapa se consideran como el auténtico principio activo del medicamento; es decir, células vivas formadoras de cartílago humano autólogo. El proceso de preparación del medicamento es muy similar al descrito para ChondroCelect® (Figura 1).
CEMTROCELL se presenta como una dosis de tratamiento individual contenida en 1 a 2 viales de plástico (tubo Falcon estéril con tapón de rosca de plástico), cada uno de los cuales contiene 0,4 ml de suspensión de condrocitos diferenciados adultos autólogos expandidos ex vivo. En cuanto a su aspecto, las células tienden a sedimentar en el fondo del tubo, formando una especie de capa blanquecina rodeada del excipiente líquido transparente e incoloro, de modo que, en el momento del implante, es necesario resuspender las células agitando suavemente el tubo hasta obtener una solución viscosa de aspecto homogéneo y color blanco-amarillento.
Eficacia y seguridad clínicas
La evidencia clínica de CEMTROCELL deriva de la experiencia de uso de la técnica de implante de condrocitos autólogos en la Clínica CEMTRO de Madrid y del uso consolidado del trasplante autólogo de condrocitos (según recoge el RD 477/2014).
La ficha técnica aprobada para el medicamento (AEMPS, 2022) recoge datos de eficacia referidos a 83 pacientes adultos de hasta 54 años de edad (56 hombres y 27 mujeres, edad mediana de 36,7 años) con lesiones de rodilla tratados en esa clínica entre 2012 y 2019. Más de dos tercios (70 %) presentaba una lesión única localizada bien en el cóndilo femoral interno (28 %) o externo (18 %) o en la rótula (19 %), con una mediana de tamaño de 4 cm2 (rango 1,2 a 15,8 cm2).
En la práctica se han empleado como las principales variables de eficacia el dolor (medido mediante la Escala Visual Analógica, EVA), la funcionalidad de la articulación (evaluada por la escala IKDC, International Knee Documentation Committee8) y las pruebas de imagen por resonancia magnética (siguiendo la escala MOCART).
Los resultados revelan que el dolor se reducía significativamente a los 2 años después del implante, con reducciones en la escala EVA de más de 5 puntos (valor basal de 6,7±2,6 y valor a los 2 años de 1,3±1,8), a la vez que la funcionalidad de la articulación mejoraba de forma clínicamente relevante: la puntuación medida de la escala IKDC aumentaba en casi 34 puntos, desde un valor basal de 40,3 (±14,4) puntos hasta 73,9 (±18,4) puntos a los 2 años desde el tratamiento. Si bien la tasa de pacientes con flexión completa de la rodilla creció significativamente a los 2 años seguimiento, no se vieron diferencias estadísticamente significativas en términos de extensión de la articulación. Desde el punto de vista radiológico se apreció una mejoría del patrón de reparación del cartílago, con una media de puntuación de la escala MOCART que a los 2 años alcanzaba los 74,7 (±19,2) puntos, en crecimiento desde los 70,4 (±9,4) puntos al año desde la administración.
En términos de seguridad, se vio que la proporción de pacientes tratados con el medicamento que sufrió derrame se redujo significativamente con un seguimiento de 2 años desde el tratamiento, sin detectarse diferencias destacables en el porcentaje de pacientes con inestabilidad. Solo un paciente presentó un evento adverso a los 2 años, dos pacientes a los 3 años, y un paciente a los 5 años desde la implantación del medicamento. El perfil toxicológico de CEMTROCELL está, pues, en línea con lo descrito para otros medicamentos basados en condrocitos autólogos, según se describe en el primer apartado de este artículo. Así, las reacciones adversas más frecuentes relacionadas con la cirugía incluyen inflamación articular posoperatoria, artralgia, pirexia, artrofibrosis y una menor amplitud de movimiento de la rodilla; todas ellas fueron en general leves y desaparecieron en las semanas siguientes a la intervención. Solo el fracaso del tratamiento y la delaminación se describen, aunque con escasa frecuencia, como las reacciones adversas más graves relacionadas con el implante.
Finalmente, se debe citar que, aunque su indicación aprobada se limita a pacientes adultos, se dispone de datos de 5 pacientes adolescentes de entre 14 y 17 años (mediana de edad de 16 años), tratados en la Clínica CEMTRO de una lesión única de rodilla localizada en ambos cóndilos o en la rótula, y de tamaño medio de 4,2 cm2 (± 1,4). Estos pacientes pediátricos también mostraron una reducción significativa del dolor según la escala EVA, desde un valor medio basal de 6,3 puntos (±2,1) hasta 1,0 puntos (±1,7) a los 2 años de seguimiento desde el tratamiento. En ese periodo, la funcionalidad de la rodilla mostró una mejoría incluso más marcada que en adultos: la puntuación de la escala IKDC creció en más de 25 puntos, desde un promedio de 39,6 (±13,6) hasta 85,3 (±23,7) puntos. Pese a que no se vieron diferencias significativas en el patrón radiológico (media del valor de MOCART de 73,8 puntos y de 73,7 puntos al año y a los 2 años, respectivamente), el perfil toxicológico de CEMTROCELL también se reveló benigno: ningún paciente presentó eventos adversos, y la tasa de derrame se redujo desde 2 pacientes a los 2 meses hasta ninguno a los 2 años desde el implante.
Aspectos innovadores
CEMTROCELL es un nuevo medicamento de terapia avanzada –producto de ingeniería tisular– cuyo principio activo son condrocitos adultos diferenciados autólogos, obtenidos a partir de una biopsia de cartílago articular y expandidos ex vivo, para los que se ha postulado que, una vez distribuidos sobre la membrana de colágeno y colocados sobre la lesión del cartílago, promueven la proliferación y diferenciación de las células cultivadas, probablemente originando la síntesis de tejido de reparación cartilaginoso de tipo hialino. En base a ello, el medicamento, que será elaborado de forma individualizada, se ha autorizado para su uso exclusivo en la Clínica CEMTRO de Madrid para la reparación –en un procedimiento quirúrgico de implantación intraarticular– de lesiones sintomáticas del cartílago de la rodilla (grado III o IV de la ICRS) en pacientes adultos. Se contraindica en pacientes con artrosis avanzada de rodilla o en quienes el fémur aún esté en crecimiento.
El fundamento farmacológico y el procedimiento de preparación del medicamento, que requiere una doble intervención quirúrgica (por la obtención inicial de una biopsia por artroscopia), son casi idénticos a lo descrito para otros medicamentos similares aprobados con anterioridad y usados con los mismos fines.
La confirmación de su eficacia deriva de la experiencia clínica en la Clínica CEMTRO, concretamente de datos de 83 pacientes adultos de mediana edad, en su mayoría con lesiones únicas del cóndilo o de la rótula, de superficie mediana de 4 cm2 y afectación superior al 50 % del grosor del cartílago.
Tomando como referencia el periodo de seguimiento de 2 años desde la administración, se ha visto que el medicamento reduce notablemente el dolor asociado a la lesión, según refleja la disminución de más de 5 puntos en la escala EVA (desde una media de casi 7 puntos basales hasta 1,3 puntos); mejora de forma relevante la funcionalidad de la articulación, con aumentos de casi 34 puntos en la escala IKDC (desde un promedio basal de 40 puntos hasta 74); y se asocia con un mejor patrón radiológico indicativo de reparación del cartílago. Asimismo, su perfil de seguridad parece encontrarse en la línea de tratamientos similares de implantación de condrocitos autólogos, y las principales reacciones adversas que se notifican en relación con el procedimiento quirúrgico de administración intraarticular son: inflamación, dolor o fibrosis de la articulación, menor amplitud de movimiento y pirexia; estas son en general leves y desaparecen con el paso del tiempo. En los 2 primeros años de seguimiento, solo un paciente había notificado eventos adversos relacionados con el medicamento, 2 a los 3 años y 1 a los 5 años: se describen como reacciones adversas el fracaso del tratamiento y la delaminación.
Sea como fuere, se trata de una evidencia clínica notablemente limitada, en contraposición con la robustez estadística que deriva de los ensayos controlados y aleatorizados. No obstante, existe una suficiente experiencia en el uso de terapias de ingeniería de tejidos basadas en condrocitos autólogos, por lo que no es esperable que haya sorpresas ni en términos de eficacia ni de seguridad después de la autorización de uso de CEMTROCELL.
En ausencia de comparaciones directas con otras estrategias terapéuticas usadas en este contexto clínico, especialmente Spherox®, no se pueden sacar conclusiones claras sobre el posicionamiento. Su carácter de tratamiento unicéntrico y el hecho de que las variables de eficacia empleadas difieren parcialmente de las investigadas con otras terapias avanzadas aprobadas hasta la fecha en indicaciones similares impiden la realización de comparaciones indirectas. A la vista de la bibliografía existente y habida cuenta del tipo de tratamiento, CEMTROCELL parece representar una alternativa interesante –aunque con un procedimiento más complejo– frente a la microfractura en el manejo de lesiones pequeñas de cartílago (< 4 cm2), sobre todo si son lesiones recientes. Puede mejorar la sintomatología y funcionalidad de la rodilla, pero, en cualquier caso, no representa una cura y la eficacia a largo plazo de las terapias a base de condrocitos autólogos ha sido puesta en entredicho (Snow et al., 2023), como en el caso del parecido ChondroCelect®, por lo que es necesario disponer de datos de mayor calidad y con mayor seguimiento para concluir sobre el beneficio clínico que realmente aporta CEMTROCELL.


Bibliografía
-
- Agencia Española de Medicamentos y Productos Sanitarios (AEMPS). Ficha técnica CEMTROCELL (condrocitos adultos autólogos). 2022. Disponible en: https://www.aemps.gob.es/investigacionClinica/terapiasAvanzadas/docs/FT-Cemtrocell.pdf.
-
- Cuéllar Rodríguez S. Condrocitos autólogos (ChondroCelect): lesiones cartilaginosas de la rodilla. Panrama Actual Med. 2013; 37(363): 388-93.
-
- Fernández Moriano C. Linfocitos T transducidos con CAR anti-CD19 (ARI-0001, Hospital Clinic de Barcelona) en leucemia linfoblástica aguda de células B. Panorama Actual Med.2021; 45(444): 608-18.
-
- Fernández Moriano C. Suspensión celular en plasma autólogo (NC1) en lesión medular traumática crónica. Panorama Actual Med.2020; 44(430): 66-74.
-
- Hoburg A, Niemeyer P, Laute V, Zinser W, Becher C, Kolombe T et al. Sustained superiority in KOOS subscores after matrix-associated chondrocyte implantation using spheroids compared to microfracture. Knee Surg Sports Traumatol Arthrosc. 2023; 31(6): 2482-93. DOI: 10.1007/s00167-022-07194-x.
-
- Ortega Polar E, Gómez González del Tánago P, Arana Zumaquero M, Alcívar Arteaga C, Panadero Carlavilla FJ. Trastornos frecuentes de cadera y rodilla. Panorama Actual Med. 2021; 45(449): 1314-25.
-
- Ruiz Antúnez S. Terapias avanzadas en patologías musculares, articulares e inmunológicas. En: Trastornos osteoarticulares, musculares e inmunológicos. Madrid: Consejo General de Colegios Oficiales de Farmacéuticos. 2018; 191-219.
-
- Snow M, Middleton L, Mehta S, Roberts A, Gray R, Richardson J et al. A Randomized Trial of Autologous Chondrocyte Implantation Versus Alternative Forms of Surgical Cartilage Management in Patients With a Failed Primary Treatment for Chondral or Osteochondral Defects in the Knee. Am J Sports Med. 2023; 51(2): 367-78. DOI: 10.1177/03635465221141907.
1 La exención hospitalaria se ha planteado como una posible herramienta que facilite la investigación y el desarrollo de terapias avanzadas por parte de organizaciones sin ánimo de lucro (instituciones académicas y hospitales), como paso previo a la solicitud de autorización de comercialización, siempre y cuando aseguren la demostración de un perfil adecuado de seguridad y eficacia clínicas.
2 El principal objetivo del RD 477/2014 fue dar un marco legal a algunos de estos productos (de terapia celular) que en el pasado no fueron considerados medicamentos pero que se encontraban en situación de uso en la práctica en algunas instituciones hospitalarias. Entre ellos se encuentran el trasplante autólogo de condrocitos, el implante de queratinocitos para tratamiento de quemados o el tratamiento de lesiones corneales con células troncales limbocorneales.
3 Cada vial del medicamento contenía 4 millones de condrocitos humanos autólogos en 0,4 ml de suspensión celular, lo que equivale a una concentración de 10 000 células por microlitro.
4 El tratamiento comprendía un procedimiento quirúrgico en 2 etapas: en la primera (unas 4 semanas antes de la implantación), se obtenía mediante artroscopia una biopsia del cartílago articular sano de la rodilla del paciente, de donde se aislaban los condrocitos (mediante digestión enzimática) para su posterior cultivo in vitro y caracterización previa a la administración de (1 × 104 células/µl); la segunda etapa consistía en la implantación de la suspensión final de condrocitos en el defecto articular por cirugía de rodilla abierta o convencional.
5 La puntuación de la escala KOOS puede oscilar de 0 a 100 puntos, donde 0 alude a la mayor severidad de los síntomas y 100 puntos se correspondería con la ausencia de síntomas.
6 El material de partida se obtiene de una biopsia tomada de una zona sana del cartílago del paciente de donde se aíslan las células y se cultivan para formar los esferoides tridimensionales, los cuales se recogen, se formulan en solución salina y se envasan. El producto final tiene un periodo de validez de 72 h, almacenado a temperaturas entre 1 y 10 °C.
7 La legislación europea establece que se considera “Medicamento de ingeniería tisular” a aquel que reúne las siguientes características: i) contiene o está formado por células o tejidos manipulados por ingeniería; y ii) del que se alega que tiene propiedades, se emplea o se administra a las personas para regenerar, restaurar o reemplazar un tejido humano. Se considerarán como “manipulados por ingeniería” a las células o tejidos que cumplan al menos una de las condiciones siguientes: i) han sido sometidos a manipulación sustancial (las incluidas en el Anexo I del Reglamento (CE) N.º 1394/2007 no se consideran sustanciales), de modo que se logran las características biológicas, funciones fisiológicas o propiedades estructurales pertinentes para la regeneración, reparación o sustitución pretendidas; o ii) las células o tejidos no están destinados a emplearse para la misma función o funciones esenciales en el receptor y en el donante.
8 La escala IKDC es un cuestionario de evaluación puramente subjetiva que examina 3 categorías: síntomas, actividad deportiva y función de la rodilla. La subescala de síntomas ayuda a evaluar cuestiones como el dolor, la rigidez, el edema y la lesión de la rodilla; funciones como subir escaleras, levantarse de una silla, ponerse en cuclillas y saltar son el objetivo de estudio de la subescala de actividad deportiva; y la subescala de función de la rodilla plantea a los pacientes una pregunta directa: ¿cómo está su rodilla ahora en comparación con cómo estaba antes de la lesión? Esta escala asigna a los pacientes una calificación funcional global de 0 a 100: las puntuaciones más altas indican niveles más altos de función y más bajos de síntomas, de modo que, si obtiene una puntuación de 100, significa que no tiene restricciones en sus actividades diarias o deportivas y que no experimenta ningún síntoma.



