AEMPS informa del cambio de dosificación de Rybelsus® (semaglutida) y los posibles errores de medicación
 Nº492
Nº492
La Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) ha informado del riesgo de cometer errores de medicación con el medicamento Rybelsus® (semaglutida), ya que se han autorizado en la Unión Europea nuevas presentaciones y dosis, debido a una nueva formulación con una biodisponibilidad mayor.
-Las nuevas presentaciones tienen la misma eficacia, seguridad y forma de administración que la formulación inicial.
-Las dos formulaciones coexistirán temporalmente en el mercado durante aproximadamente cuatro meses.
-Los pacientes deben recibir una información adecuada para evitar confusiones o errores de medicación.
-Para la dispensación de las nuevas presentaciones será necesaria una actualización de la prescripción por parte del profesional sanitario.
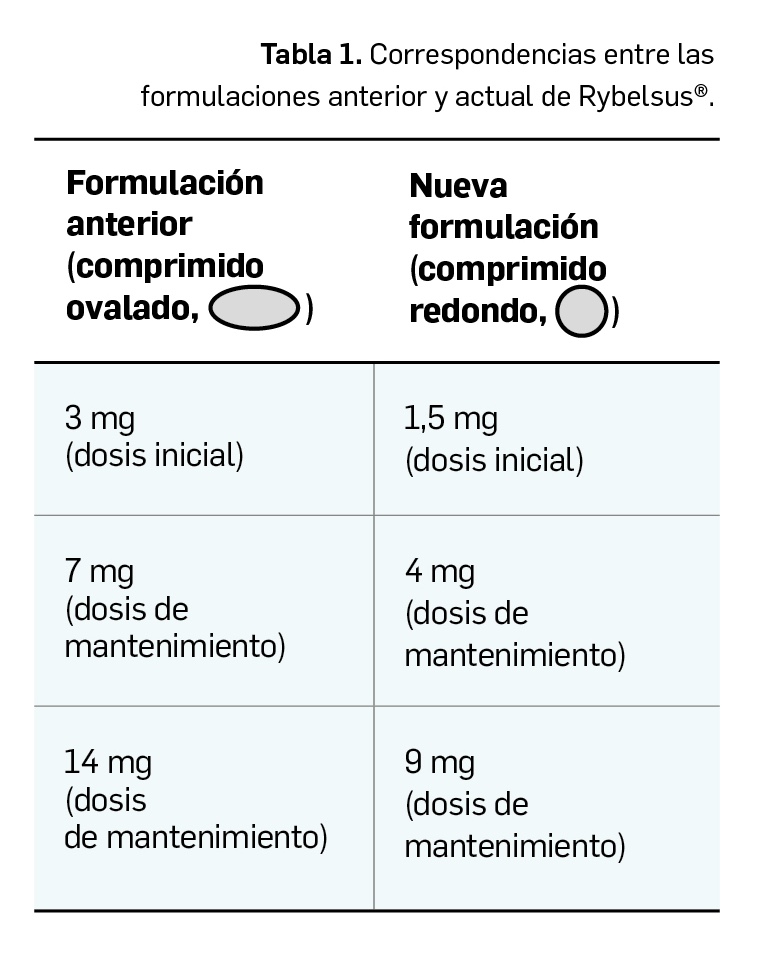
La Agencia Española de Medicamentos y Productos Sanitarios (AEMPS), ha informado recientemente que la empresa comercializadora del medicamento Rybelsus®, Novo Nordisk Pharma, S.A., ha desarrollado una nueva formulación que permite reducir la dosis de principio activo, consiguiendo la misma exposición al medicamento y el mismo efecto (AEMPS, 2026). Es decir, se logra que las antiguas presentaciones y las nuevas sean bioequivalentes y, por tanto, cada una de las presentaciones iniciales (comprimidos de 3 mg, 7 mg, 14 mg) se sustituyen por su correspondiente nueva presentación (comprimidos de 1,5 mg, 4 mg, 9 mg), manteniéndose la misma vía de administración.
El medicamento Rybelsus® contiene el principio activo semaglutida y está indicado en el tratamiento de pacientes adultos con diabetes mellitus tipo 2, que no han sido controlados adecuadamente, como complemento de la dieta y el ejercicio, en combinación con otros medicamentos para el tratamiento de la diabetes.
El cambio actual se produce porque los excipientes utilizados en esta nueva formulación permiten aumentar la biodisponibilidad del principio activo semaglutida, es decir, aumentar la absorción por el organismo del paciente. Este cambio en la formulación ha sido evaluado favorablemente por la Agencia Europea de Medicamentos, EMA (del inglés, European Medicines Agency) una vez que ha sido demostrado a través de un ensayo clínico pertinente.
Adicionalmente, el comprimido de la nueva formulación también se ha modificado la forma con respecto a la presentación inicial, y en todos los casos está grabado el número de la dosis en el comprimido. Sin embargo, el color en los envases que indican los distintos niveles de dosificación se ha mantenido similar.
Durante 4 meses que durará el periodo de transición, al coexistir ambas formulaciones, podría dar lugar a confusión y suponer un riesgo de errores de medicación a pacientes que utilicen regularmente este medicamento. Estos errores podrían causar una mayor exposición a semaglutida, lo que podría provocar efectos adversos gastrointestinales, como náuseas, vómitos y diarrea, entre otros.
La información del medicamento (prospecto y ficha técnica) se ha actualizado para explicar la diferencia entre las dos formulaciones y permitir a los lectores identificar las dosis equivalentes.
Es importante tener en cuenta que las presentaciones son bioequivalentes, pero la receta médica de las antiguas presentaciones no es válida para las nuevas. Por tanto, los profesionales sanitarios deberán ir actualizando las prescripciones a las nuevas dosis de manera progresiva.
Recomendaciones para profesionales sanitarios
Teniendo en cuenta que será siempre muy útil la intervención del farmacéutico en el momento de la dispensación de estas presentaciones, se deben tener presentes estas recomendaciones:
a) Si el paciente ya está tomando Rybelsus®, debe actualizar la prescripción a las nuevas presentaciones, consultando a su médico prescriptor.
b) Asegúrese de que el paciente comprende el cambio de medicación para evitar errores de medicación durante la prescripción y la dispensación.
c) Los inicios de tratamiento con Rybelsus® deben prescribirse con la nueva formulación.
Consulte la Tabla 1 anterior de equivalencias para saber cuál es la nueva dosificación que le corresponde a cada paciente.
Recomendaciones a los padres y / o cuidadores de los pacientes pediátricos
La dispensación de medicamentos con paracetamol con o sin receta médica solo será en farmacias, por lo que debe recibir asesoramiento.
a) Seguir las instrucciones de administración indicadas en el prospecto del medicamento, en caso de duda consulte con un profesional sanitario.
b) La dosis recomendada de paracetamol en mililitros (ml) se calcula en función de la concentración del medicamento y el peso actual de la niña o niño.
c) Prestar especial atención si procede de otro país y está habituado a administrar paracetamol en solución oral, porque en su país de origen puede que la concentración de paracetamol sea menor a la que está disponible en España; por lo tanto, podría necesitar menos volumen (ml) para administrar la misma dosis.
d) Utilizar correctamente el método de administración de la solución oral (jeringa dosificadora o gotas) ya que puede variar según el medicamento. Si tiene dudas, consulte con el profesional farmacéutico.
e) En caso de administrar accidentalmente una cantidad superior a la recomendada, acuda a un centro médico, aunque no presente síntomas, ya que estos pueden aparecer de forma tardía, generalmente a partir del tercer día tras la ingestión.
Recomendaciones a los pacientes
La dispensación de medicamentos con Rybelsus® con receta médica solo será en farmacias, por lo que los pacientes deben recibir asesoramiento:
a) Si ya está tomando Rybelsus®, continúe su tratamiento con normalidad hasta terminar toda la medicación que tenga en su domicilio.
b) Cuando tenga que renovar su prescripción, su médico le hará una receta médica con las nuevas dosificaciones. Debe saber que su aspecto y dosis se han cambiado, pero el medicamento sigue actuando igual que en la presentación anterior.
c) Consulte la Tabla 1 anterior de equivalencias si tiene dudas sobre cuál es la nueva dosificación que le corresponde.
d) Siga las instrucciones de administración indicadas en el prospecto del medicamento. En caso de duda consulte con su profesional farmacéutico.
Si se equivoca con la dosis, puede sufrir efectos adversos gastrointestinales. Si lo necesita, acuda a su profesional sanitario. Puede notificar los efectos adversos a su médico, farmacéutico, enfermero, o directamente como paciente puede notificar mediante la app www.notificaRAM.es, tal como se indica en el prospecto.




