Garantía farmacéutica en la cadena de suministro
 Nº490
Nº490
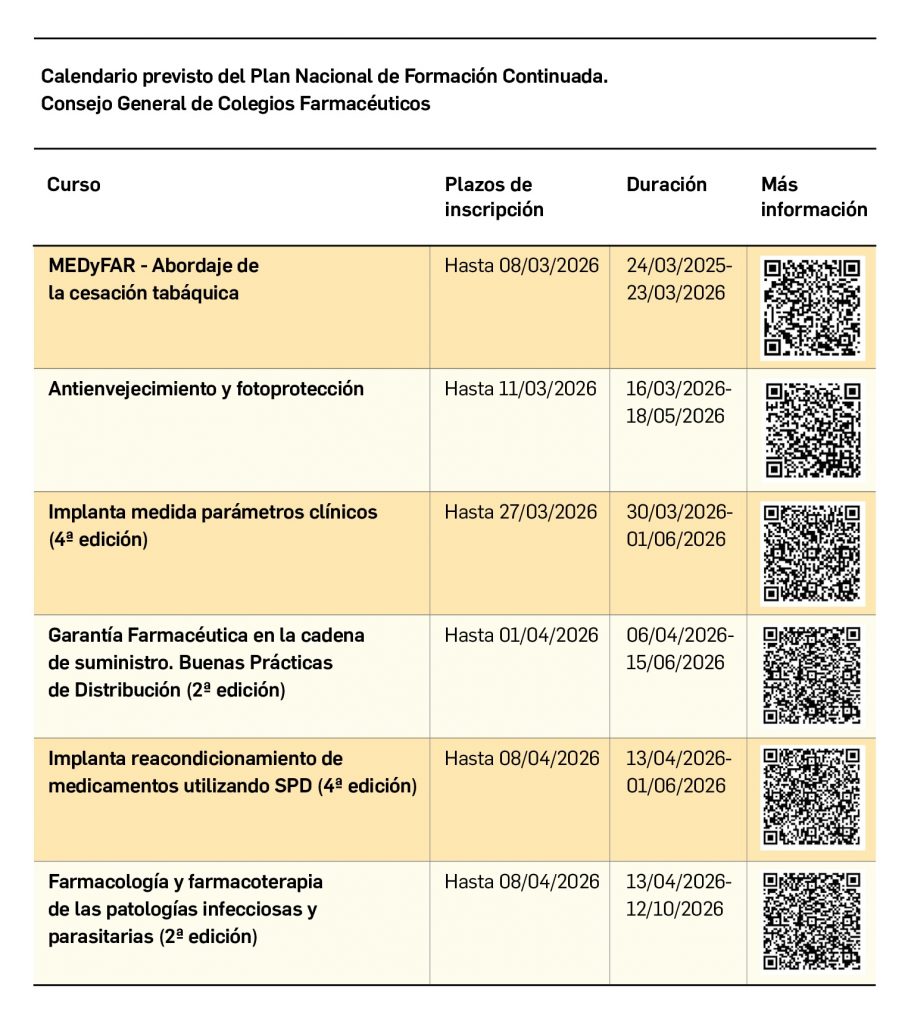
Las BPD constituyen el pilar fundamental en el que se basan las actividades de distribución mayorista e intermediación de medicamentos de uso humano en la Unión Europea (UE). Su marco legal viene definido por dos textos clave:
- Las Directrices de la Comisión Europea de 5 de noviembre de 2013 (2013/C 343/01), que establecen los requisitos técnicos y operativos para garantizar que los medicamentos se almacenen y transporten en condiciones adecuadas, manteniendo en todo momento su calidad, integridad y trazabilidad.
- El Real Decreto 782/2013, de 11 de octubre, que regula en España la distribución de medicamentos de uso humano e incorpora a la práctica nacional las obligaciones derivadas de la normativa europea.
El objetivo central de estas directrices es proteger al paciente y al sistema sanitario frente a riesgos derivados de manipulaciones inadecuadas o de la introducción de medicamentos falsificados en la cadena de suministro. Para ello, las BPD fijan requisitos que abarcan desde la autorización de los almacenes mayoristas, hasta los procedimientos de recepción, almacenamiento, transporte, gestión de devoluciones, controles de calidad, trazabilidad documental y cooperación con las autoridades competentes.
El control de la cadena de distribución, desde la fabricación o importación hasta la dispensación al paciente, constituye un elemento esencial para asegurar la calidad de los medicamentos y garantizar que las condiciones de conservación, transporte y suministro se mantienen en todo momento dentro de los parámetros establecidos.
La actividad de distribución deberá garantizar un servicio de calidad, siendo su función prioritaria y esencial el abastecimiento a las oficinas de farmacia y a los servicios de farmacia legalmente autorizados en el territorio nacional.
Las entidades de distribución y, en su caso, los laboratorios farmacéuticos que distribuyan directamente sus productos estarán obligados a:
- Disponer de locales y equipos dotados de medios personales, materiales y técnicos para garantizar la correcta conservación y distribución de los medicamentos, con plena garantía para la salud pública.
- Garantizar la observancia de las condiciones generales o particulares de conservación de los medicamentos y especialmente el mantenimiento de la cadena de frío en toda la red de distribución mediante procedimientos normalizados.
- Mantener unas existencias mínimas de medicamentos que garanticen la adecuada continuidad del abastecimiento.
- Asegurar plazos de entrega, frecuencia mínima de repartos, asesoramiento técnico farmacéutico permanente y medios de apoyo a oficinas y servicios de farmacia.
- Cumplir servicios de guardia y prevención de catástrofes.
- Disponer de un plan de emergencia que garantice la aplicación efectiva de cualquier retirada del mercado ordenada por las autoridades sanitarias competentes.
- Tener implantado un sistema de alertas que cubra todas las farmacias del territorio de su ámbito de actuación.
- Cumplir con las normas de BPD que hayan sido promovidas o autorizadas por las administraciones sanitarias competentes y a colaborar con estas para asegurar una prestación farmacéutica de calidad y el cumplimiento de las demás obligaciones que vengan impuestas por disposición legal o reglamentaria.
En este sentido, el Real Decreto 782/2013, de 11 de octubre, sobre distribución de medicamentos de uso humano, tiene por objeto regular las actividades de distribución e intermediación.
Dentro de este marco normativo, las entidades de distribución reguladas incluyen los almacenes mayoristas de distribución, los almacenes por contrato y los almacenes de medicamentos bajo control o vigilancia aduanera, todas ellas obligadas a garantizar la calidad del producto en todas las fases de la cadena de suministro, desde la salida del fabricante hasta la oficina de farmacia o el servicio de farmacia hospitalaria. Para su funcionamiento, además de contar con la autorización correspondiente, estas entidades deben disponer de un certificado de cumplimiento de Buenas Prácticas de Distribución (BPD) en vigor, emitido por la autoridad competente, que avala la idoneidad de sus procesos y sistemas de control.
Las diferentes empresas que pueden realizar distribución farmacéutica en España se dividen en:
Entidades de distribución de medicamentos:
- Almacenes mayoristas.
- Almacenes por contrato: terceros.
- Almacenes de medicamentos bajo control o vigilancia aduanera.
Entidades dedicadas a la intermediación de medicamentos, también conocidos como brókers.
Entidades que están habilitadas per se para la distribución:
- Laboratorios Titulares de la Autorización de Comercialización, TAC.
- Laboratorios farmacéuticos fabricantes/importadores (BPD).
La publicación del Real Decreto 782/2013 sobre distribución de medicamentos de uso humano supone el hito más importante en la actividad realizada hasta esa fecha por la distribución farmacéutica, generándose la obligación de actualizar las Prácticas de Correcta Distribución que tenía implementadas, a las BPD, de obligado cumplimiento tanto por las entidades de distribución de medicamentos, como por los laboratorios farmacéuticos que realicen actividades de distribución.
La Directiva 92/25/CEE define en su primer artículo la distribución al por mayor de medicamentos como “toda actividad que consista en obtener, conservar, proporcionar o exportar medicamentos, excluido el despacho de medicamentos al público; estas actividades serán realizadas con fabricantes o sus depositarios, importadores, otros distribuidores al por mayor o con los farmacéuticos y personas autorizadas o facultadas, en el Estado miembro de que se trate, para dispensar medicamentos al público”.
Cada eslabón de la cadena sanitaria (laboratorio, distribuidora, oficina o servicio de farmacia) cuenta con una normativa propia para garantizar la calidad del medicamento en todo momento, destacando las Buenas Prácticas de Producción en los laboratorios fabricantes y las Buenas Prácticas de Distribución (BPD).