Evolocumab REPATHA® (Amgen)
 Nº390
Nº390
Resumen
El evolocumab es un anticuerpo monoclonal con propiedades hipolipemiantes, que actúa uniéndose a la proteína PCSK9, provocando una reducción de la degradación intracelular de los receptores de las lipoproteínas de baja densidad (LDL) y, en consecuencia, una reducción de los niveles de LDL-colesterol (cLDL) en sangre. Ha sido autorizado para el tratamiento de adultos con hipercolesterolemia primaria (familiar heterocigótica y no familiar) o dislipidemia mixta, como complemento a la dieta en combinación con una estatina o con una estatina y otros tratamientos hipolipemiantes en pacientes que no consiguen alcanzar los niveles objetivo de cLDL con la dosis máxima tolerada de estatina, o bien solo o en combinación con otros tratamientos hipolipemiantes en pacientes intolerantes a las estatinas o en los que las estatinas están contraindicadas. También está indicado en adultos y adolescentes a partir de 12 años con hipercolesterolemia familiar homocigótica en combinación con otros tratamientos hipolipemiantes. Considerando la relevancia sanitaria de las indicaciones autorizadas para el evolocumab, la escasez de alternativas farmacológicas, la magnitud de los efectos obtenidos con el evolocumab, la persistencia de su efecto durante periodos prolongados, el amplio margen de seguridad mostrado hasta ahora, la incorporación de un nuevo mecanismo de acción hipolipemiante que actúa de forma potente y directa sobre los procesos bioquímicos de eliminación de cLDL del torrente circulatorio y, finalmente, la cómoda posología (inyección subcutánea convencional cada dos o cuatro semanas), este nuevo medicamento es valorado como una innovación importante.
HIPERCOLESTEROLEMIA
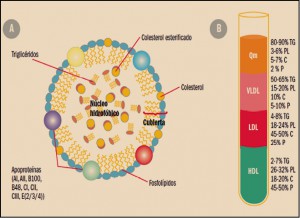
Los lípidos son sustancias que nuestro organismo utiliza como almacén de energía y que desempeñan importantes funciones (formación de las membranas celulares, modificación de proteínas, producción de hormonas, etc.). Por su carácter liposoluble, estas moléculas precisan, para su transporte en el medio acuoso que constituye el plasma, de un vehículo adecuado. Colesterol, triglicéridos y fosfolípidos se transportan en el plasma formando macrocomplejos en los que las moléculas más hidrófobas se disponen en el centro y se recubren de otras hidrófilas, como fosfolípidos y apolipoproteína. Estos macrocomplejos son lo que conocemos como lipoproteínas (Figura 1), entre las que se diferencian varios tipos (de baja densidad –LDL–, de alta densidad –HDL–, etc.) en función de la composición del núcleo lipófilo y el tipo de apoproteínas que presentan (algunas de las cuales constituyen la tarjeta de presentación de las lipoproteínas a su receptor). Los niveles plasmáticos de lipoproteínas reflejaran por tanto los de los lípidos que contienen (Díez, 2012).
Las dislipemias son alteraciones del metabolismo lipídico que conducen a desviaciones de los valores normales de las lipoproteínas o los lípidos en el organismo. Se denominan primarias cuando se deben a una alteración genética o a una dieta inadecuada, y secundarias cuando están relacionadas con patologías que alteran el metabolismo lipídico, como son la diabetes mellitus, trastornos renales, hipotiroidismo o la administración de algunos medicamentos (p. ej., los inhibidores de la proteasa, la ciclosporina o las tiazidas).
El incremento de los niveles de colesterol unido a LDL (cLDL) y la disminución de los de colesterol unido a HDL (cHDL) constituyen, junto con la hipertensión y el tabaquismo, los principales factores de riesgo modificables para la aterosclerosis, una enfermedad sistémica que afecta a las arterias alterándolas progresivamente y formando placas esclerosadas que llegan a reducir la luz vascular (estenosis), conduciendo a situaciones con mayor o menor grado de isquemia del área afectada, y cuya rotura puede desencadenar la activación plaquetaria, dando lugar a trombosis o embolia, que pueden causar un infarto o un accidente cerebrovascular.
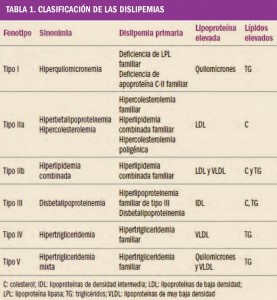
Las dislipemias han sido objeto de distintos sistemas de clasificación. La de Fredrickson (Tabla 1) es la más útil en cuanto a terapéutica, pero debemos saber que en cada uno de los tipos se pueden encontrar distintas enfermedades (primarias o secundarias a otras patologías) que pueden dar lugar a la alteración de los niveles de un tipo de lipoproteína. La reducción del cLDL y los triglicéridos retrasa la progresión e incluso puede reducir la placa de ateroma. Todos los datos disponibles indican que el control de las dislipemias es esencial en la prevención primaria y secundaria de las enfermedades cardiovasculares.
La hiperlipidemia familiar es un trastorno genético en el que se agrupan varias patologías. La más común es la hipercolesterolemia familiar, caracterizada por la presencia de elevadas concentraciones sanguíneas de cLDL y por el desarrollo prematuro de enfermedades cardiovasculares. Está asociada a la existencia de mutaciones del gen codificador del receptor de LDL (R-LDL) en el 95% de los casos, aunque también se asocia con mutaciones de los genes codificadores de Apolipoproteína B (ApoB) y de la PCSK9 (Proprotein convertase subtilisin/kexin type 9), un enzima codificado que se une al R-LDL presente en los hepatocitos, facilitando su internalización y degradación.
En su forma heterocigótica, la hipercolesterolemia familiar tiene una prevalencia en la Unión Europea de 1:200 a 1:500 y, a pesar de tratamiento hipolipemiante intensivo, presenta una tasa de mortalidad doble de lo normal. Por su parte, la forma homocigótica es aún mucho más grave, cursando con niveles de cLDL y colesterol total extraordinariamente elevados, lo que determina una alta mortalidad incluso en edad infantil y juvenil; afortunadamente, es mucho más infrecuente que la forma heterocigótica, con una prevalencia entre 1:300.000 y 1:1.000.000.
En el caso de las dislipemias secundarias, el primer paso debe ser el tratamiento de la patología de base y, en todos los casos, controlar la dieta y favorecer un estilo de vida saludable –ejercicio, abandonar el tabaco, moderar el consumo de alcohol– y, si fuese necesario, administrar tratamiento farmacológico.
Los ácidos grasos constituyen la base de los lípidos del organismo. Son ácidos orgánicos con cadenas hidrocarbonadas de diferente longitud y grado de saturación. Estos ácidos grasos se esterifican con otras sustancias como glicerol y ácido fosfórico, dando lugar entre otros productos a triglicéridos y fosfolípidos, o bien son metabolizados a esteroles, dando lugar al colesterol. Como ya se ha dicho, al ser inmiscibles en el medio acuoso de la sangre, los lípidos necesitan acoplarse a un vehículo adecuado. Los ácidos grasos no esterificados se asocian a la albumina, pero los restantes constituyen las lipoproteínas. Este sistema permite movilizar los triglicéridos desde el intestino y el hígado hasta los puntos de utilización o almacenamiento (tejido adiposo y musculo) y transportar el colesterol allí donde se necesita, por ejemplo para la síntesis de membranas, la producción de hormonas esteroideas o la síntesis de ácidos biliares.
Las lipoproteínas (Tabla 2) se clasifican según su densidad (a mayor densidad, mayor contenido en proteínas, y a mayor diámetro, mayor contenido de lípidos) y, como veremos, cada tipo ejerce distintas funciones:
- Quilomicrones: se forman en el intestino, contienen apoproteína B48 y transportan fundamentalmente los triglicéridos, los fosfolípidos y el colesterol procedentes de la dieta y de la síntesis en el epitelio intestinal. En los tejidos periféricos ricos en lipoproteína lipasa (LPL), liberan ácidos grasos.
- Lipoproteínas de muy baja densidad (VLDL, very low density lipoproteins): contienen apoproteína B (ApoB), C y E y transportan triglicéridos y colesterol, sintetizados en el hígado, hacia los tejidos periféricos, cediendo igualmente ácidos grasos en tejidos periféricos.
- Lipoproteínas de baja densidad (LDL, low density lipoproteins): proceden de las VLDL (presentan por tanto las mismas apoproteínas) y representan el principal sistema de transporte del colesterol hacia las células de los tejidos periféricos.
- Lipoproteínas de alta densidad (HDL, high density lipoproteins): contienen fundamentalmente apoproteína A (ApoA), C y E. Transportan el colesterol cedido por las células de los tejidos periféricos al hígado. Es, por tanto, un mecanismo bioquímico hipocolesterolemiante.
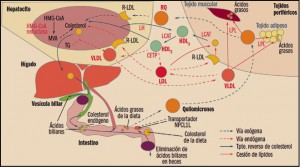
Los enterocitos liberan los lípidos absorbidos a la linfa en forma de quilomicrones ricos en triglicéridos. En los capilares del tejido adiposo y muscular esquelético, ricos en lipoproteína lipasa (LPL), los lípidos contenidos en los quilomicrones son hidrolizados a ácidos grasos, que son asimilados por las células de estos tejidos, donde se almacenan, constituyendo un depósito de energía, o se emplean como materia prima para la síntesis de otros lípidos (Figura 2). Los quilomicrones remanentes, que no han perdido su colesterol, sufren un proceso de endocitosis en el hígado.
El colesterol hepático, ya sea de origen endógeno o exógeno, puede ser esterificado y almacenado, excretarse en la bilis como colesterol libre o ser transformado en ácidos biliares, constituir nuevas lipoproteínas o incorporarse a las membranas plasmáticas de los hepatocitos. Aproximadamente el 80% del colesterol endógeno procede de síntesis hepática y se libera a la circulación en forma de VLDL; a nivel de los capilares del musculo esquelético y del tejido graso, las VLDL sufren el ataque de la LPL, que hidroliza los triglicéridos y libera ácidos grasos, que son captados por los tejidos y convierten a las VLDL en LDL. Los niveles elevados de LDL y su oxidación forman parte de la base etiopatogénica de la aterosclerosis. Las LDL circulantes son reconocidas por receptores presentes en las membranas celulares (R-LDL), produciéndose su endocitosis al interior celular. Allí se convierten en sustrato de enzimas lisosomales, cediendo colesterol libre.
Las HDL se sintetizan en el hígado y en el intestino, pero también en la sangre circulante a partir de apoproteínas y fosfolípidos procedentes de la hidrolisis de los quilomicrones y las VLDL por la LPL. Las HDL son responsables del denominado transporte inverso de colesterol, es decir, del que se produce desde las células periféricas al hígado. Esta es la razón por la que los niveles altos de cHDL se asocian a un menor riesgo de cardiopatía isquémica. Estas HDL nacientes captan el colesterol libre de la superficie de las membranas celulares en tejidos periféricos y, por acción de la lecitincolesterol-acil transferasa (LCAT), van aumentando su contenido en colesterol esterificado y su tamaño, convirtiéndose en partículas de HDL2 que pueden acceder al hepatocito para ceder el colesterol, o bien convertirse en HDL3 por acción de la lipasa hepática, que libera triglicéridos. El colesterol esterificado no atraviesa las membranas celulares y se intercambia, gracias a la proteína de transferencia de esteres de colesterol (CETP), por los triglicéridos de las VLDL y LDL.
Según la Organización Mundial de la Salud (OMS), las enfermedades cardiovasculares se encuentran entre las 10 primeras causas de muerte en todos los países del mundo, y en el caso concreto de la aterosclerosis, resulta la primera causa de muerte e incapacidad en los países desarrollados. En la actualidad, se considera un proceso inmunoinflamatorio crónico de origen multigénico y multifactorial, que comienza tempranamente por una disfunción del endotelio vascular y modificaciones oxidativas de los lípidos sanguíneos atrapados en el subendotelio vascular. Los lípidos depositados en las lesiones ateroscleróticas provienen fundamentalmente de las LDL circulantes, que ingresan en la pared vascular a través de este endotelio lesionado o disfuncional.
La enfermedad se desarrolla de forma intermitente en el tiempo; se observa que el crecimiento de las placas es discontinuo, se intercalan periodos de inactividad con otros de rápida evolución y todo ello es modulado por factores ambientales y genéticos. El resultado final es que, como consecuencia de una serie de factores etiopatogénicos, tiene lugar la aparición y desarrollo de lesiones con mayor o menor contenido lipídico, presencia de colágeno, fibras elásticas y calcio, que, en casos avanzados, pueden sufrir complicaciones (rotura o fisura de la placa, con el evidente riesgo de trombosis). La localización y el grado de desarrollo de estas lesiones dan lugar a las diferentes formas de enfermedad aterosclerótica, que se caracterizaran por unos síntomas y signos que corresponden, bien a la obliteración de la luz vascular con disminución del flujo y aparición de isquemia crónica, bien a la obstrucción de dicha luz por rotura de la placa y aparición de fenómenos trombóticos (debido a que el núcleo lipídico de la placa es altamente trombogénico y desencadena la activación de las cascadas de la coagulación y de la adhesión y agregación plaquetarias), con manifestaciones de isquemia aguda.
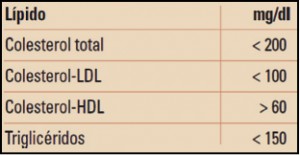
La prevención y tratamiento de las dislipemias deben contemplarse como parte fundamental de la prevención de la enfermedad cardiovascular. Como tal, sus objetivos deben ajustarse atendiendo al riesgo cardiovascular que presenta el paciente concreto. A lo largo de numerosos y amplios ensayos clínicos, se ha evidenciado que la reducción de los niveles séricos de colesterol total y de cLDL comporta una reducción del riesgo cardiovascular, por lo que esto se convierte en objetivo prioritario del tratamiento, al que pueden seguir los valores de otras fracciones lipídicas asociadas a la aterosclerosis.
Existe abundante documentación clínica que demuestra que los niveles plasmáticos altos de colesterol se relacionan con un aumento de la incidencia de la morbilidad y mortalidad cardiovasculares. La aparentemente obvia conclusión de que el tratamiento hipolipemiante estaría justificado en todos los casos de pacientes con riesgo cardiovascular, sin embargo, es todavía objeto de polémica y está lejos de haberse demostrado esta máxima terapéutica para todos los agentes hipolipemiantes. En general, con cifras de disminución del LDL-colesterol del orden del 25-30% hay un retardo significativo en la progresión de la arteriosclerosis en arteria coronaria y carotidea (la regresión de las lesiones se produce pocas veces). Los objetivos terapéuticos están recogidos en la tabla 3.
Por tanto, el criterio principal subrogado1 para juzgar la eficacia del tratamiento es el descenso de la fracción LDL y el aumento de la fracción HDL. Actualmente, hay una tendencia a evitar los tratamientos farmacológicos hipocolesterolemiantes en pacientes jóvenes sin factores de riesgo cardiovascular, e intensificarlos en cambio en pacientes que hayan sufrido un episodio coronario o presenten, en general, un nivel de riesgo coronario y/o cerebrovascular de moderado a elevado. Algunas normas fijan objetivos del tratamiento en términos de niveles de LDL y en función de la presencia o no de enfermedad coronaria y de la existencia de factores adicionales de riesgo. En cualquier caso, la terapia hipolipemiante parece evolucionar a tratamientos cada vez más selectivos, pero también más intensivos.
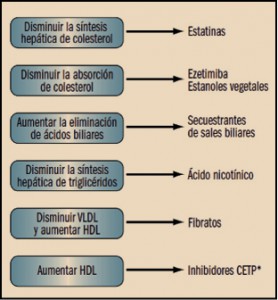
Los denominados inhibidores de la HMG-CoA reductasa, más comúnmente referidos como estatinas (atendiendo al sufijo común de esos fármacos), actúan inhibiendo competitivamente uno de los enzimas claves en el proceso de síntesis del colesterol en el organismo. Producen una reducción rápida e intensa de colesterol total (15-30%) y de cLDL (25-60%), un descenso moderado de triglicéridos (10-25%) y ligero ascenso (4-10%) de cHDL. La experiencia es de buena tolerancia aunque ocasionalmente producen aumento de las transaminasas séricas (que revierten al suspender el tratamiento) o miositis.
La inhibición de la HMG-CoA reductasa produce una activación de las proteínas reguladoras SREBP (sterol regulatory elements-binding proteins), que activan la transcripción de proteínas e incrementan la expresión del gen del receptor de LDL y un aumento en la cantidad de receptores funcionales en el hepatocito, dando lugar a una mayor eliminación de las LDL circulantes, lo que disminuye las concentraciones de cLD. El orden de potencia hipolipemiante de las estatinas a nivel equimolecular es: pitavastatina > rosuvastatina > atorvastatina > simvastatina > pravastatina = lovastatina > fluvastatina. Sin embargo, cuando se utilizan dosis equivalentes, el efecto terapéutico es similar. Al doblar la dosis de cualquier estatina, el aumento relativo en la reducción de cLDL es, en general, del 6-7%. El efecto sobre los triglicéridos es mayor en los sujetos con triglicéridos >250 mg/dl, en los que se alcanza el 35% de reducción. Las estatinas actúan rápidamente, inhibiendo la enzima limitante en pocas horas; asimismo, más del 90% del efecto reductor de cLDL se consigue las primeras cuatro semanas de tratamiento, sin que sea haya evidenciado tolerancia farmacológica con el tratamiento crónico.
Aparte de sus efectos sobre el perfil lipídico, las estatinas tienen otros efectos cardiovasculares beneficiosos, especialmente sobre la pared arteria y que explicarían el beneficio adicional no atribuible a la reducción del cLDL observado en muchos estudios de intervención (efectos pleiotrópicos). Al inhibir la HMG-CoA reductasa, las estatinas interfieren en la formación de isoprenoides a partir del mevalonato. Como consecuencia de esto, la prenilación de las proteínas G (Rho, Rac, Rab y Ras) se reduce. La prenilación de estas moléculas es necesaria para su anclaje a la membrana celular y, así, poder ejercer su mecanismo de acción relacionado con la migración, la diferenciación y la proliferación celular. A través de estos potenciales efectos sobre las proteínas celulares, las estatinas pueden tener una serie de propiedades antiateroscleróticas y antitrombóticas, como la inhibición del crecimiento de la célula muscular lisa, la adhesión celular, la activación plaquetaria y la secreción de proteína C reactiva, entre otras. Por todo ello, actualmente se considera a las estatinas como tratamiento hipolipemiante de referencia (Cuéllar, 2011).
Los derivados del ácido clofíbrico reducen fundamentalmente los niveles de triglicéridos (30-50%), y consecuentemente cVLDL, y aumentan los de cHDL (10-20%). La acción reductora sobre colesterol total (10-20%) y cLDL (5-10%) es comparativamente mucho menor, y muy variable según el fármaco. Los medicamentos más modernos, únicos que permanecen en el mercado, como el fenofibrato y bezafibrato, etc., son más activos que el clofibrato sobre el colesterol y fracciones lipídicas relacionadas. Por su parte, gemfibrozilo tiene poco efecto sobre el colesterol, pero en cambio tiene una acción más pronunciada sobre triglicéridos y en ciertos casos produce una elevación significativa de la fracción cHDL.
Entre los adsorbentes o secuestrantes de sales biliares, colestipol, colesevelam y colestiramina son polímeros de intercambio aniónico, mientras que el detaxtrano es un derivado del dextrano mucho menos difundido y documentado. Se encuentran entre los medicamentos hipolipemiantes más antiguos, aunque no por ello su eficacia es cuestionada. De hecho, forman parte de todas las estrategias terapéuticas hipocolesterolemiantes, tanto solos como en asociación con estatinas. Reducen los niveles de cLDL en un 10-30% y en combinación con ácido nicotínico o con estatinas dicha reducción puede alcanzar el 60%. Actúan uniéndose a los ácidos biliares presentes en el intestinal, formando complejos inabsorbibles que son eliminados con las heces y, por tanto, impiden la reabsorción de dichos ácidos biliares. A medida que la reserva orgánica de estos se agota, el enzima colesterol 7a hidrolasa experimenta una regulación al alza, incrementado la tasa de conversión de colesterol en ácidos biliares, lo que a su vez provoca un aumento de la demanda de colesterol por parte de los hepatocitos, dando lugar a un incremento tanto de la expresión como de la actividad de la HMG-Coa reductasa, así como del número de receptores hepáticos de LDL. Estos efectos compensatorios potencian la eliminación de cLDL de la sangre y, por consiguiente, reducen sus niveles.
A pesar de su eficacia probada y de que no son absorbidos en el tracto intestinal, se asocian con una elevada tasa de discontinuidad en el tratamiento, debido fundamentalmente a las molestias gastrointestinales, en especial el estreñimiento que llega a afectar al 40% de los pacientes tratados. Además, producen flatulencia, borborigmos y calambres intestinales.
El interés por los aceites poliinsaturados de pescado surgió de estudios epidemiológicos indicativos de que poblaciones con dietas ricas en pescado (esquimales, japoneses) tienen una incidencia de enfermedades cardiovasculares significativamente inferior a otros grupos de población con consumo equivalente de grasas animales o vegetales. Los preparados de aceite de pescado son mezclas de los ácidos eicosapentaenoico y docosaexaenoico, en la que la acción farmacológica principal la ejerce el primero. El segundo actúa fundamentalmente de reserva transformándose lentamente en ácido eicosapentaenoico, aunque puede tener funciones biológicas aún no bien conocidas. Aunque a dosis terapéuticas ambos se comportan como hipolipemiantes, desarrollan significativos otros efectos preventivos cardiovasculares cuya naturaleza es compleja, porque modifican la proporción de los diversos tipos de prostaglandinas del organismo, lo que puede traducirse en acción vasodilatadora e inhibición de la agregación plaquetaria.
La ezetimiba es un agente hipolipemiante que reduce la absorción intestinal del colesterol procedente de la dieta y de la secreción biliar. En dosis terapéuticas, es capaz de reducirla en más de un 50%. En términos generales, la ezetimiba reduce los niveles de cLDL en un 17-20% en monoterapia, y en más del 40% en combinación con estatinas. Tiene una acción reductora moderada sobre triglicéridos (10%) e incrementa modestamente los niveles de HDL (5-10%). Actúa situándose en las microvellosidades del intestino delgado, inhibiendo la captación del colesterol por los enterocitos, a través de un mecanismo aún no bien dilucidado.
ACCIÓN Y MECANISMO
El evolocumab es un anticuerpo monoclonal con propiedades hipolipemiantes, que actúa uniéndose a la proteína PCSK9, provocando una reducción de la degradación intracelular de los receptores de LDL-colesterol y, en consecuencia, una reducción de los niveles de LDL-colesterol (cLDL) en sangre. Ha sido autorizado para el tratamiento de adultos con hipercolesterolemia primaria (familiar heterocigótica y no familiar) o dislipemia mixta, como complemento a la dieta en combinación con una estatina o con una estatina y otros tratamientos hipolipemiantes en pacientes que no consiguen alcanzar los niveles objetivo de cLDL con la dosis máxima tolerada de estatina, o bien solo o en combinación con otros tratamientos hipolipemiantes en pacientes intolerantes a las estatinas o en los que las estatinas están contraindicadas. También está indicado en adultos y adolescentes a partir de 12 años con hipercolesterolemia familiar homocigótica en combinación con otros tratamientos hipolipemiantes.
La PCSK9 (Proprotein Convertase Subtilisin/Kexin type 9) es un enzima codificado por el gen del mismo nombre, que se une al receptor de LDL presente en los hepatocitos. Cuando la PCSK9 se une al receptor de LDL (R-LDL) presente en la membrana, este sufre un proceso de internalización, pasando al citoplasma donde es degradado. Al bloquear la PCSK9, el evolocumab favorece la permanencia de dichos receptores en la superficie de los hepatocitos y su actividad para retirar las moléculas de LDL-colesterol circulantes en el torrente sanguíneo. Además de los efectos sobre los niveles de cLDL, el evolocumab facilita también la reducción de los de colesterol total, apolipoproteína B (ApoB), cVLDL, triglicéridos y lipoproteína a (Lp(a)).
ASPECTOS MOLECULARES
El evolocumab es un anticuerpo monoclonal enteramente humano de la clase IgG2 que se une selectivamente y con gran afinidad a la proteína PCSK9, inactivándola biológicamente. Presenta la característica estructura en forma de Y, constituida por dos cadenas peptídicas pesadas (con 441 aminoácidos cada una) y otras dos ligeras (con 215 aminoácidos cada una), interconectadas mediante 18 puentes disulfuro (-S-S-), tanto inter como intracatenarios. Presenta un punto de N-glucosilación (en el aminoácido Asn291 de cada una de las dos cadenas pesadas), pero no presenta O-glucosilación. El peso molecular total del evolocumab (no glucosilado) es de 141,8 kDa. La desglucosilación del evolocumab no parece afectar de forma significativa a su potencia biológica.
EFICACIA Y SEGURIDAD CLÍNICAS
La eficacia y la seguridad clínicas del evolocumab han sido adecuadamente contrastadas en las indicaciones autorizadas mediante varios ensayos clínicos de fase 3 (confirmatorios de eficacia y seguridad), aleatorizados, multicéntricos, doblemente ciegos (abiertos, en algunos casos) y controlados con placebo y comparadores activos, fundamentalmente ezetimiba.
En concreto, se dispone de ensayos clínicos en hiperlipidemia primaria (familiar heterocigótica y no familiar) y dislipemia mixta (pacientes adultos entre 18 y 80 años), tanto en monoterapia tanto en combinación con estatinas y, eventualmente, otros hipolipemiantes, así como en pacientes con intolerancia a las estatinas. La hiperlipidemia primaria (familiar heterocigótica y no familiar) fue definida como la existencia de niveles elevados de cLDL aislados, mientras que se consideró como dislipemia mixta la combinación de niveles elevados de cLDL y triglicéridos (≥150 mg/dL; 1,7 mmol/L) o de bajos niveles de cHDL (≤40 mg/dL, 1,0 mmol/L en varones; ≤50 mg/dL, 1,3 mmol/L en mujeres). La hipercolesterolemia grave fue definida como la existencia de niveles séricos de cLDL ≥160 mg/dL; 4,1 mmol/L estando bajo tratamiento con estatinas o de ≥240 mg/dL; 6,2 mmol/L sin tratamiento con estatinas. También ha sido estudiado en pacientes con hipercolesterolemia familiar homocigótica (pacientes entre 12 y 80 años).
La variable primaria de eficacia utilizada en estos estudios fue la variación porcentual media experimentada en los niveles plasmáticos de cLDL a las 10 y 12 semanas desde el inicio del tratamiento. Como variables secundarias de determinaron las variaciones porcentuales y absolutas de ApoB, colesterol total, cHDL, ApoA1, lipoproteína a, triglicéridos, cVLDL, así como determinaciones de seguridad; asimismo, en algunos estudios se determinaron los porcentajes de pacientes que experimentaron una reducción ≥50% en sus niveles de cLDL o que consiguieron alcanzar un nivel determinado (≤70 o 100 mg/dL, según el estudio). En los estudios a largo plazo, se determinaron las variaciones porcentuales de los parámetros lipídicos a las 52 semanas.
Los estudios tuvieron una duración que osciló entre 12 semanas y cinco años, utilizándose dosis subcutáneas (SC) de evolocumab de 140 mg cada dos semanas o de 420 mg cada mes. Los características y resultados de los ensayos clínicos controlados están recogido en las tablas 4 y 5 en hiperlipidemia primaria y dislipemia mixta, y 6 en hipercolesterolemia familiar homocigótica.
|
Tabla 4. Estudios clínicos de fase 3 y 12 semanas de duración con evolocumab en hiperlipidemia primaria y dislipemia mixta |
||||
|
Parámetro |
Hiperlipidemia primaria familiar y no familiar |
Hiperlipidemia primaria familiar y no familiar |
Hiperlipidemia primaria familiar y no familiar; intolerantes a estatinas(1) |
Hiperlipidemia primaria familiar |
|
Tratamiento de base |
Ninguno |
Estatinas ± Ezetimiba |
Hipolipemiantes (no estatinas ni ezetemiba) |
Estatinas ± Ezetimiba |
|
Tratamientos comparados |
Evolocumab 140 mg/2 sem Evolocumab 420 mg/mes Ezetimiba 10 mg/24 h oral Placebo |
Evolocumab 140 mg/2 sem Evolocumab 420 mg/mes Ezetimiba 10 mg/24 h oral Placebo |
Evolocumab 140 mg/2 sem Evolocumab 420 mg/mes Ezetimiba 10 mg/24 h oral |
Evolocumab 140 mg/2 sem Evolocumab 420 mg/mes Placebo |
|
Pacientes (finalizaron) |
614 (97%) |
1896 (96%) |
307 (95%) |
329 (94%) |
|
Edad (media) |
53 años |
60 años |
62 años |
51 años |
|
Sexo (mujeres) |
66% |
46% |
46% |
42% |
|
Coronariopatía |
<1% |
23% |
29% |
31% |
|
Diabetes tipo 2 |
<1% |
16% |
20% |
7% |
|
Hipertensión |
29% |
57% |
59% |
33% |
|
Historial familiar de patología cardiovascular |
10% |
20% |
32% |
59% |
|
cLDL basal media (ayunas) |
143 mg/dL (3,7 mmolL) |
108 mg/dL (2,1 mmolL) |
193 mg/dL (5,0 mmolL) |
155 mg/dL (4,0 mmolL) |
|
Determinación de la variable primaria |
10 y 12 semanas |
10 y 12 semanas |
10 y 12 semanas |
10 y 12 semanas |
|
Variación cLDL (vs. placebo) |
Evolocumab (140): -57% Evolocumab (420): -55% |
Evolocumab (140): -74% Evolocumab (420): -61% |
- |
Evolocumab (140): -61% Evolocumab (420): -66% |
|
Variación cLDL (vs. ezetimiba) |
Evolocumab (140): -39% Evolocumab (420): -38% |
Evolocumab (140): -44% Evolocumab (420): -43% |
Evolocumab (140): -38% Evolocumab (420): -39% |
- |
|
Variación colesterol total (2) |
Evolocumab (140): -25% Evolocumab (420): -25% |
Evolocumab (140): -41% Evolocumab (420): -40% |
Evolocumab (140): -24% Evolocumab (420): -26% |
Evolocumab (140): -42% Evolocumab (420): -44% |
|
Variación Triglicéridos |
Evolocumab (140): -9% Evolocumab (420): -9% |
Evolocumab (140): -17% Evolocumab (420): -23% |
Evolocumab (140): -6% (ns) Evolocumab (420): -9% |
Evolocumab (140): -23% Evolocumab (420): -17% |
|
Variación cVLDL |
Evolocumab (140): -7% (ns) Evolocumab (420): -10% (ns) |
Evolocumab (140): -18% Evolocumab (420): -22% |
Evolocumab (140): -4% (ns) Evolocumab (420): -7% (ns) |
Evolocumab (140): -23% Evolocumab (420): -16% |
|
Variación cHDL |
Evolocumab (140): +6% Evolocumab (420): +4% |
Evolocumab (140): +6% Evolocumab (420): +8% |
Evolocumab (140): +5% Evolocumab (420): +6% |
Evolocumab (140): +8% Evolocumab (420): +9% |
|
Variación relación CT/cHDL |
Evolocumab (140): -29% Evolocumab (420): -28% |
Evolocumab (140): -45% Evolocumab (420): -46% |
Evolocumab (140): -27% Evolocumab (420): -30% |
Evolocumab (140): -47% Evolocumab (420): -49% |
|
Variación ApoB |
Evolocumab (140): -34% Evolocumab (420): -35% |
Evolocumab (140): -56% Evolocumab (420): -56% |
Evolocumab (140): -32% Evolocumab (420): -35% |
Evolocumab (140): -49% Evolocumab (420): -55% |
|
Variación ApoA1 |
Evolocumab (140): +3% Evolocumab (420): +4% |
Evolocumab (140): +3% Evolocumab (420): +5% |
Evolocumab (140): +5% Evolocumab (420): +3% (ns) |
Evolocumab (140): +7% Evolocumab (420): +5% |
|
Variación relación ApoB/ApoA1 |
Evolocumab (140): -35% Evolocumab (420): -37% |
Evolocumab (140): -56% Evolocumab (420): -58% |
Evolocumab (140): -35% Evolocumab (420): -36% |
Evolocumab (140): -53% Evolocumab (420): -56% |
|
Variación Lp(a) |
Evolocumab (140): -22% Evolocumab (420): -20% |
Evolocumab (140): -30% Evolocumab (420): -27% |
Evolocumab (140): -24% Evolocumab (420): -25% |
Evolocumab (140): -31% Evolocumab (420): -31% |
|
Referencia |
MENDEL-2 (Koren, 2014) |
LAPLACE-2 (Robinson, 2014) |
GAUSS-2 (Stroes, 2014) |
RUTHERFORD-2 (Raal, 2015) |
Nota: Salvo que se indique lo contrario, los datos indican diferencias vs. placebo. Todas las diferencias en la variable primaria observadas con los datos del medicamento de referencia y los del comparador fueron estadísticamente significativas, salvo aquellas notadas con (ns). (1) No hubo brazo placebo; todas las comparaciones se hicieron respecto a ezetimiba. (2) Salvo que se indique lo contrario, todas las comparaciones se indican respecto al placebo.
|
Tabla 5. Estudios clínicos de fase 3 de larga duración con evolocumab en hiperlipidemia primaria y dislipemia mixta |
||
|
Parámetro |
Hiperlipidemia primaria familiar y no familiar |
Hiperlipidemia primaria familiar y no familiar(1) |
|
Tratamiento de base |
Dieta ± atrovastatina ± ezetimiba |
Tratamiento estándar |
|
Tratamientos comparados |
Evolocumab 420 mg/mes Placebo |
Evolocumab 140 mg/2 sem Evolocumab 420 mg/mes |
|
Pacientes |
901 |
2928 |
|
Duración |
52 semanas |
124 semanas |
|
cLDL basal media (ayunas) |
104 mg/dL (2,7 mmolL) |
124 mg/dL (3,2 mmolL) |
|
Determinación de la variable primaria |
52 semanas |
12 y 24 semanas |
|
Variación cLDL (vs. placebo) |
Evolocumab (420): -59% |
Evolocumab (140): -54% Evolocumab (420): -53% |
|
Variación colesterol total |
Evolocumab (420): -33% |
- |
|
Variación Triglicéridos |
Evolocumab (420): -12% |
- |
|
Variación cVLDL |
Evolocumab (420): -29% |
- |
|
Variación cHDL |
Evolocumab (420): +5% |
- |
|
Variación relación CT/cHDL |
Evolocumab (420): -37% |
- |
|
Variación ApoB |
Evolocumab (420): -44% |
- |
|
Variación ApoA1 |
Evolocumab (420): +3% |
- |
|
Variación relación ApoB/ApoA1 |
Evolocumab (420): -46% |
- |
|
Variación Lp(a) |
Evolocumab (420): -22% |
- |
|
Referencia |
DESCARTES (Blom, 2014) |
OSLER-2 (Sabatine, 2015) |
Nota: Salvo que se indique lo contrario, los datos indican diferencias vs. placebo. Todas las diferencias en la variable primaria observadas con los datos del medicamento de referencia y los del comparador fueron estadísticamente significativas. (1) Estudio abierto, sin brazo placebo; las diferencias se expresan con respecto a los valores basales.
|
Tabla 6. Estudios clínicos de fase 3 con evolocumab en hipercolesterolemia familiar homocigótica |
||
|
Parámetro |
Hipercolesterolemia familiar homocigótica |
|
|
Tratamientos comparados |
Evolocumab 420 mg/mes Placebo |
Evolocumab 420 mg/mes(1) |
|
Pacientes |
49 |
98 |
|
Duración |
12 semanas |
5 años |
|
Edad (media) |
31 años (20% <18 años) |
- |
|
cLDL basal media (ayunas) |
348 mg/dL (9,0 mmolL) |
321 mg/dL (8,3 mmolL) |
|
Determinación de la variable primaria |
12 semanas |
24 semanas |
|
Variación cLDL |
Evolocumab (420): -31% |
Evolocumab (420): -21% |
|
Referencia |
TESLA-B (Raal, 2015) |
TAUSSIG (EMA, 2015) |
Nota: Todas las diferencias en la variable primaria observadas con los datos del medicamento de referencia y los del comparador fueron estadísticamente significativas. (1) Estudio abierto.
Desde el punto de vista de la seguridad, el evolocumab presenta un perfil toxicológico benigno, con adversos poco frecuentes y generalmente leves o moderados, transitorios y tratables fácilmente. Los eventos adversos más frecuentemente descritos en los ensayos clínicos de fase 3 son: nasofaringitis (3,2% con la dosis evolocumab de 140 mg/2 sem y 5,8% con la de 420 mg/mes; 4,0% con ezetimiba y 2% con placebo), infección del tracto respiratorio superior (1,8%; 4,1%; 2,3% y 3,0%), dolor de espalda (2,3%; 3,6%; 2,3% y 3,8%), cefalea (2,6%; 3,4%; 3,6% y 2,9%), dolor de espalda (2,3%; 3,6%; 2,3% y 3,8%), síntomas gripales (1,4%; 2,9%; 1,6% y 3,1%), dolor muscular (1,7%; 2,5%; 4,9% y 2,4%), dolor articular (2,0%; 2,4%; 2,2% y 2,7%) y náusea (1,7%; 2,4%; 2,2% y 2,0%).
La incidencia de eventos adversos graves fue del 2,8% vs. 2,4% con placebo y 2,1% con ezetimiba. Se procedió a la suspensión del tratamiento en el 1,9% de los tratados con evolocumab, 1,6% con placebo y 2,3% con ezetimiba.
ASPECTOS INNOVADORES
El evolocumab es un anticuerpo monoclonal con propiedades hipolipemiantes, que actúa uniéndose a la proteína PCSK9, provocando una reducción de la degradación intracelular de los receptores de LDL-colesterol y, en consecuencia, una reducción de los niveles de LDL-colesterol en sangre. La PCSK9 (Proprotein Convertase Subtilisin/Kexin type 9) es un enzima codificado por el gen del mismo nombre, que se une al receptor de LDL-colesterol presente en los hepatocitos. Cuando la PCSK9 se une al receptor de LDL (R-LDL) presente en la membrana, este sufre un proceso de internalización, pasando al citoplasma donde es degradado. Al bloquear la PCSK9, el evolocumab favorece la permanencia de dichos receptores en la superficie de los hepatocitos y su actividad para retirar las moléculas de cLDL circulantes en el torrente sanguíneo. Además de reducir los niveles de cLDL, el evolocumab facilita también la disminución de los de colesterol total, apolipoproteína B (ApoB), cVLDL, triglicéridos y lipoproteína a, incrementando modestamente los de CHDL y ApoA1.
Ha sido autorizado para el tratamiento de adultos con hipercolesterolemia primaria (familiar heterocigótica y no familiar) o dislipidemia mixta, como complemento a la dieta en combinación con una estatina o con una estatina y otros tratamientos hipolipemiantes en pacientes que no consiguen alcanzar los niveles objetivo de C-LDL con la dosis máxima tolerada de estatina, o bien solo o en combinación con otros tratamientos hipolipemiantes en pacientes intolerantes a las estatinas o en los que las estatinas están contraindicadas. También está indicado en adultos y adolescentes a partir de 12 años con hipercolesterolemia familiar homocigótica en combinación con otros tratamientos hipolipemiantes.
Los datos clínicos disponibles son abundantes y metodológicamente robustos, con resultados contundentes en relación a la variable clínica principal, el descenso de los niveles séricos de cLDL. En este sentido, la documentación clínica muestra en los pacientes con hipercolesterolemia primaria (familiar heterocigótica y no familiar) o dislipidemia mixta descensos del 60-70% en relación al placebo y del 40% vs. ezetimiba al cabo de 12 semanas, tanto en monoterapia como asociación a otros hipolipemiantes (estatinas, ezetimiba, etc.), en pacientes que, en muchos casos eran intolerantes o refractarios al tratamiento con las dosis de máximas de estatinas de alta potencia (atorvastatina y rosuvastatina). Asimismo, otros parámetros lipídicos potencialmente adversos desde el punto de vista del riesgo cardiovascular experimentan descensos notables, tales como ApoB (50-54% vs. placebo y 34% vs. ezetimiba), colesterol total (37-41% y 24%) y triglicéridos (15-20% y 3-6%), con aumentos ligeros pero estadísticamente significativos de los niveles de cHDL (6-8% y 5-7%). Estos descensos fueron mantenidos en periodos de más de dos años, al menos.
Asimismo, en pacientes con hipercolesterolemia familiar homocigótica se ha reportado una reducción del 15-32% en los niveles de cLDL al cabo de 12 y 24 semanas, incluyendo un pequeño número de pacientes entre 12 y 18 años, con persistencia del efecto durante más de dos años, al menos. Como en el caso anterior, también se vieron afectados favorablemente otros parámetros lipídicos.
Los valores de los niveles séricos de los parámetros lipídicos empleados en estos ensayos clínicos son variables subrogadas de los efectos sobre el riesgo cardiovascular; es decir, tales valores estarían directamente ligados a un descenso proporcional de dicho riesgo patológico. Aunque es obvio que lo ideal sería que en los propios ensayos clínicos se hubieran determinado incidencia de trastornos cardiovasculares, es preciso indicar que tal observación requeriría periodos de tiempo mucho mayores que los habitualmente empleados en estos ensayos clínicos y, por otro lado, existe una abundante documentación clínica que demuestra tal relación con muchos otros agentes hipolipemiantes, en particular con las estatinas. Además, ya hay algunos datos clínicos incipientes que asocian directamente el empleo de evolucumab con una reducción significativa del 53% (0,95 vs. 2,18%) en la incidencia de eventos cardiovasculares al cabo de un año, en relación con la terapia estándar (Sabatine, 2015).
Un aspecto muy relevante a tener en consideración es el perfil benigno de seguridad que ha mostrado el evolocumab en los ensayos clínicos realizados hasta ahora, con eventos adversos escasos, leves y clínicamente irrelevantes, equiparables a los controles utilizados (incluyendo el placebo). Esto viene corroborado con la tasa de suspensión del tratamiento por eventos adversos, que fue del 1,9% con evolocumab, 1,6% con placebo y 2,3% con ezetimiba. Los eventos adversos más habitualmente reportados son nasofaringitis, infección del tracto respiratorio superior, dolor de espalda, cefalea, dolor de espalda, síntomas gripales, dolor muscular, dolor articular y náusea, con incidencias que van del 2% al 6%, prácticamente en línea con el placebo y la ezetimiba. La dosificación de 420 mg al mes se asocia con una ligera mayor incidencia de eventos adversos que la de 140 cada dos semanas.
La hiperlipidemia familiar es un trastorno genético en el que se agrupan varias patologías. La más común es la hipercolesterolemia familiar, caracterizada por la presencia de elevadas concentraciones sanguíneas de cLDL y por el desarrollo prematuro de enfermedades cardiovasculares. Está asociada a la existencia de mutaciones del gen codificador del receptor de LDL (95% de los casos), aunque también se asocia puntualmente con mutaciones de los genes codificadores de Apolipoproteína B (ApoB) y de la PCSK9. En su forma heterocigótica, la hipercolesterolemia familiar tiene una prevalencia en la Unión Europea de 1:200 a 1:500 y, a pesar de tratamiento hipolipemiante intensivo, presenta una tasa de mortalidad doble de lo normal. Por su parte, la forma homocigótica es aún mucho más grave, cursando con niveles de cLDL y colesterol total extraordinariamente elevados, lo que determina una alta mortalidad incluso en edad infantil y juvenil; afortunadamente, es mucho más infrecuente que la forma heterocigótica, con una prevalencia entre 1:300.000 y 1:1.000.000.
Evidentemente, el evolocumab no es una primera opción de tratamiento de una hiperlipidemia leve o moderada; para ello existen numerosas alternativas mucho más experimentadas, que han demostrado plenamente su eficacia no solo farmacológica – en términos de niveles lipídicos – sino preventiva del riesgo cardiovascular. Sin embargo, las indicaciones autorizadas para el evolocumab incluyen a pacientes de alto riesgo cardiovascular que prácticamente carecen de otras opciones farmacológicas, al ser resistentes o intolerantes a los más potentes hipolipemiantes actualmente disponibles (estatinas) en su mayor dosificación.
Deben considerarse la relevancia sanitaria de las indicaciones autorizadas para el evolocumab, la escasez de alternativas farmacológicas, la magnitud de los efectos obtenidos con el evolocumab, la persistencia de su efecto durante periodos prolongados, el amplio margen de seguridad mostrado hasta ahora, la incorporación de un nuevo mecanismo de acción hipolipemiante que actúa de forma potente y directa sobre los procesos bioquímicos de eliminación de cLDL del torrente circulatorio y, finalmente, la cómoda posología (inyección subcutánea convencional cada dos o cuatro semanas). En definitiva, este conjunto de aspectos favorables determina que este nuevo medicamento sea valorado como una innovación importante.
|
VALORACIÓN |
|
|
EVOLOCUMAB
|
|
|
Grupo Terapéutico (ATC): C10AX. SISTEMA CARDIOVASCULAR. Agentes modificadores de lípidos: otros. |
|
|
Indicaciones autorizadas: Tratamiento de adultos con hipercolesterolemia primaria (familiar heterocigótica y no familiar) o dislipidemia mixta, como complemento a la dieta en combinación con una estatina o con una estatina y otros tratamientos hipolipemiantes en pacientes que no consiguen alcanzar los niveles objetivo de C-LDL con la dosis máxima tolerada de estatina, o bien solo o en combinación con otros tratamientos hipolipemiantes en pacientes intolerantes a las estatinas o en los que las estatinas están contraindicadas. También está indicado en adultos y adolescentes a partir de 12 años con hipercolesterolemia familiar homocigótica en combinación con otros tratamientos hipolipemiantes. |
|
|
VALORACIÓN GLOBAL: INNOVACIÓN IMPORTANTE. Aportación sustancial a la terapéutica estándar |
♣ ♣ ♣ |
|
Novedad clínica: Mejora la eficacia clínica con relación al tratamiento estándar. |
⇑ |
|
Novedad molecular: Mecanismo de acción innovador frente al de los tratamientos previamente disponibles para la misma o similar indicación terapéutica. |
⇑ |
|
Novedad toxicológica: Mejora el perfil toxicológico con relación a la terapia estándar. |
⇑ |
BIBLIOGRAFÍA
Bibliografía
- Blom DJ, Hala T, Bolognese M, Lillestol MJ, Toth PD, Burgess L; DESCARTES Investigators.A 52-week placebo-controlled trial of evolocumab in hyperlipidemia. N Engl J Med. 2014; 370(19): 1809-19. doi: 10.1056/NEJMoa1316222.
- Consejo General de Colegios Oficiales de Farmacéuticos. Bot PLUS WEB. https://botplusweb.portalfarma.com/
- Cuéllar Rodríguez S. Colesevelam (Choletagel®) en hipercoelsterolemia primaria. Panorama Actual Med 2011; 35(348): 951-8.
- Díez González LM, Fernández del Pozo de Salamanca MB.Fármacos hipolipemiantes. En: Terapéutica farmacológica de los trastornos cardiovasculares, renales y hematológicos. Madrid: Consejo General de Colegios Oficiales de Farmacéuticos; 2012. pp. 157-78.
- European Medicines Agency (EMA). Repatha®.European Public Assessment Report (EPAR). EMA/577183/2015; EMEA/H/C/003766. http://www.ema.europa.eu/docs/en_GB/document_library/EPAR_-_Public_assessment_report/human/003766/WC500191400.pdf
- Keating GM.Evolocumab: A Review in Hyperlipidemia. Am J Cardiovasc Drugs. 2016; 16(1): 67-78. doi: 10.1007/s40256-015-0153-0.
- Koren MJ, Lundqvist P, Bolognese M, Neutel JM, Monsalvo ML, Yang J; MENDEL-2 Investigators.Anti-PCSK9 monotherapy for hypercholesterolemia: the MENDEL-2 randomized, controlled phase III clinical trial of evolocumab. J Am Coll Cardiol. 2014; 63(23): 2531-40. doi: 10.1016/j.jacc.2014.03.018.
- Raal FJ, Honarpour N, Blom DJ, Hovingh GK, Xu F, Scott R, Wasserman SM, Stein EA; TESLA Investigators.Inhibition of PCSK9 with evolocumab in homozygous familial hypercholesterolaemia (TESLA Part B): a randomised, double-blind, placebo-controlled trial. Lancet. 2015; 385(9965): 341-50. doi: 10.1016/S0140-6736(14)61374-X.
- Raal FJ, Stein EA, Dufour R, Turner T, Civeira F, Burgess L, et al; RUTHERFORD-2 Investigators.PCSK9 inhibition with evolocumab (AMG 145) in heterozygous familial hypercholesterolaemia (RUTHERFORD-2): a randomised, double-blind, placebo-controlled trial. Lancet. 2015; 385(9965): 331-40. doi: 10.1016/S0140-6736(14)61399-4.
- Robinson JG, Nedergaard BS, Rogers WJ, Fialkow J, Neutel JM, Ramstad D, et al; LAPLACE-2 Investigators.Effect of evolocumab or ezetimibe added to moderate- or high-intensity statin therapy on LDL-C lowering in patients with hypercholesterolemia: the LAPLACE-2 randomized clinical trial. JAMA. 2014; 311(18): 1870-82. doi: 10.1001/jama.2014.4030.
- Sabatine MS, Giugliano RP, Wiviott SD, Raal FJ, Blom DJ, Robinson J, et al; Open-Label Study of Long-Term Evaluation against LDL Cholesterol (OSLER) Investigators.Efficacy and safety of evolocumab in reducing lipids and cardiovascular events. N Engl J Med. 2015; 372(16): 1500-9. doi: 10.1056/NEJMoa1500858.
- Stroes E, Colquhoun D, Sullivan D, Civeira F, Rosenson RS, Watts GF; GAUSS-2 Investigators.Anti-PCSK9 antibody effectively lowers cholesterol in patients with statin intolerance: the GAUSS-2 randomized, placebo-controlled phase 3 clinical trial of evolocumab. J Am Coll Cardiol. 2014; 63(23): 2541-8. doi: 10.1016/j.jacc.2014.03.019.
1 El concepto de criterio subrogado parte del paralelismo demostrado empíricamente entre un parámetro bioquímico (biomarcador) y unas consecuencias clínicas determinadas. En este caso, los niveles de cLDL y colesterol total (entre otros) son considerados como un indicador subrogado del riesgo cardiovascular en sus diversas manifestaciones patológicas (infarto de miocardio, accidente cerebrovascular, etc.).
Artículos relacionados
-
31 Mar 2026Medicamentos con nuevos principios activos o biosimilares Medicamentos con nuevos principios activos o biosimilares
-
27 Feb 2026Medicamentos con nuevos principios activos o biosimilares Medicamentos con nuevos principios activos o biosimilares
-
23 Dic 2025Medicamentos con nuevos principios activos o biosimilares Medicamentos con nuevos principios activos o biosimilares